Иммунитет
Содержание:
- Иммунитет: зачем он нужен?
- Что такое иммунограмма?
- Нормальные показатели
- Как регулируется иммунный ответ?
- Схема Th1 ответа. Эффекторы клеточного ответа.
- Что выяснили российские учёные
- Иммунитет гуморальный
- Диагностика и результаты иммунологического анализа
- Типы иммунитета: какие есть?
- Виды иммунного ответа
- Нюансы случая
- Другие факторы иммунитета
Иммунитет: зачем он нужен?
Иммунная система отвечает за антигенный гомеостаз. В принятой в науке терминологии иммунитетом именуют невосприимчивость к определенному типу патологических микроскопических форм жизни и продуктов их жизнедеятельности, а также ядов, генерируемых животным. Иммунная система принимает участие в опознании и деструкции самых разных клеточных структур – бактерий и вирусов, паразитарных, простейших, грибковых, опухолевых. Иммунный ответ, возникающий при этом – это реакция на инвазию.
Эволюция – особенность, присущая любой форме жизни, но особенно ярко она прослеживается, если наблюдать за микроорганизмами. Свойства микроскопических форм жизни постоянно совершенствуются, и единственным эффективным ответом на это со стороны макроорганизмов оказалось формирование иммунитета разных видов. Впрочем, иммунитет не единственное, что защищает человека. Немалую роль играют факторы, не допускающие инвазию. К примеру, проникновение патологической микрофлоры в человеческий организм затруднено за счет эпителиальных ресничек, кожных покровов, слизистых, а также высокой кислотности желудочной среды.
Что такое иммунограмма?
Это специальный анализ крови, который позволяет оценить количество различных иммунных клеток, вырабатываемых ими антител и ряда других веществ, свидетельствующих о состоянии защитных систем организма. В зависимости от цели исследования и возможностей лаборатории, количество исследуемых параметров может существенно варьироваться. Расширенное исследование позволяет изучить более 25 различных показателей – такой анализ выявляет даже скрытые нарушения, которые невозможно обнаружить стандартными методиками.
Иммунитет человека можно условно разделить на два звена – «медленное» (гуморальное) и «быстрое» (клеточное). Быстрое звено реагирует практически сразу после попадания возбудителя болезни (вируса, гриба, бактерии, простейших и т.д.) в организм. В задачу этой группы клеток входят следующие функции:
- Поглотить и «переварить» вредоносного агента;
- Презентировать или «рассказать» о патогенном микроорганизме другим иммунным клеткам, которые не могут самостоятельно его обнаружить;
- Уничтожить наибольшее количество выявленных микробов;
- Бороться с различными опухолями и аутоиммунными процессами – еще одна важная функция иммунитета, которая часто не позволяет организму самостоятельно справиться с болезнью.
После того, как «быстрое» звено поглотило чужеродное тело и рассказало о нем «медленному» звену, запускается медленный процесс создания и выброса антител в кровь. Антитела – это вещества, уничтожающие определенный вид патогенного агента. Они очень специфичны и, в большинстве случаев, помогают организму окончательно справиться с имеющимся заболеванием. В среднем, продолжительность их создания составляет 2-3 недели.
Показатели иммунограммы отражают работу каждого из звеньев защиты. Именно на основании их изменений делается вывод об отсутствии/наличии иммунодефициты, о варианте нарушения и оптимальном методе терапии.
| Звено иммунитета, исследуемый параметр | Функция |
| Цитотоксические Т-клетки (CD3+, CD8+) | Распознавание вредоносных микроорганизмов и их уничтожение |
| Т-хелперы (CD4+) | «Рассказывают» о наличии патогена другим клеткам-защитникам, играют существенную роль в формировании длительного иммунитета. |
| Т-супрессоры (CD8+) | Регуляция активности защитных систем, предохраняют организм от развития аутоиммунных реакций (когда вырабатываются антитела против здоровых тканей) |
| Т-клетки с рецептором для ИЛ-2 (CD25+) | |
| Носители маркера апоптоза (CD95+) | Контроль скорости процесса самоуничтожения клеток |
| В-клетки (CD+, 19CD+) | Отвечают за выработку специфических антител. В большинстве случаев, именно благодаря данному пулу клеток происходит полное выздоровление.
Защищают организм от повторного заражения той же самой инфекцией, в течение определенного времени. |
| Иммуноглобулин G | Антитела, вырабатываемые В-клетками. При связывании с вредоносным микробом – разрушают его стенку, вследствие чего наступает гибель. |
| Иммуноглобулин M | |
| Иммуноглобулин A | |
| Иммуноглобулин | Отвечает за развитие любых аллергических реакций. |
| стественные/натуральные киллеры (CD16+) или NK-клетки | Обеспечивают естественный противоопухолевый иммунитет |
| Клетки с HLA маркером | Отражает активность работы иммунных механизмов |
| Фагоцитоз | Распознавание, поглощение и презентация Т-клеткам вредоносных агентов |
| Реакция торможения миграции лейкоцитов (сокращенно – РТМЛ) | Лабораторный тест, отражающий работу клеточного звена. |
| НСТ-тест | Позволяет оценить активность фагоцитоза |
| Комплемент | Предотвращает формирование больших по размеру иммунных комплексов (соединений вредоносных частиц с антителами). Участвует в нейтрализации микробов |
В некоторых случаях, доктор может порекомендовать дополнить анализ исследованием содержания интерлейкинов в крови – это специальные вещества, которые обеспечивают взаимосвязь различных компонентов защитных систем. При нарушении их выработки также могут формироваться иммунодефицитные состояния.
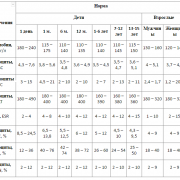
Нормальные показатели
Если у пациента повышен ИРИ, то это может быть признаком серьезных заболеваний. Однако невозможно поставить диагноз только лишь по данным иммунограммы. В данном случае необходимо пройти дополнительное обследование. При аутоиммунных патологиях больному показан длительный прием кортикостероидов и иммуносупрессоров, а также диспансерное наблюдение.
Что делать, если ИРИ снижен? Такой показатель является признаком ослабления защитных сил организма. Существуют ли препараты для повышения иммунорегуляторного индекса? Если снижение ИРИ спровоцировано инфекционной патологией или хроническими болезнями, то иммунитет самостоятельно приходит в норму после выздоровления или достижения ремиссии. В некоторых случаях пациентам назначают иммуномодуляторы:
- «Виферон»;
- «Полиоксидоний»;
- «Арбидол»;
- «Иммунал»;
- «Циклоферон».
Однако такие препараты можно принимать только по назначению и под контролем врача. Со временем организм привыкает к иммуномодуляторам, и эффективность таких лекарств уменьшается. Злоупотребление иммуностимулирующими препаратами может привести к истощению собственной иммунной системы.
Увеличение IgA происходит при хронических болезнях печени, аутоиммунных заболеваниях, миеломе, гломерулонефрите, алкогольной интоксикации. Снижению концентрации иммуноглобулина А способствуют физиологические изменения у ребенка до 6 месяцев, циррозное поражение печени, лучевая болезнь, терапия иммунодепрессантами, отравление организма химическими веществами.
Рост содержания IgG отмечается при аутоиммунных заболеваниях, миеломе, ВИЧ-инфекции, мононуклеозе инфекционной этиологии, инфекционных патологиях. Снижение иммуноглобулина G происходит в результате физиологических изменений у ребенка в возрасте до 6 месяцев, лучевой болезни, отравления химическими веществами, терапии иммунодепрессантами.
Антинуклеарные антитела повышаются при аутоиммунных патологиях, нефрите, хроническом гепатите, васкулите. Показатель АСЛО растет при острой форме гломерулонефрите, ревматизме, рожистом воспалении, скарлатине и инфицировании стрептококками. Антиспермальные антитела повышены при риске бесплодия. Показатель MAR-теста увеличен при вероятном бесплодии мужчины. Показатели АТ-ТГ и АТ-ТПО увеличиваются при аутоиммунном тиреоидите, болезни Грейвса, синдроме Дауна и Тернера.
Анализ на ЦИК (циркулирующие иммунные комплексы) назначают при: обследовании на наличие аутоиммунных патологий и дефицита комплемента, иммунопатогенетических поражениях почек, артритах различной этиологии, персистирующей инфекции. Циркулирующие иммунные комплексы повышены при остром инфицировании организма, персистирующей инфекции, аутоиммунных патологиях, аллергическом альвеолите, гломерулонефрите в острой форме, местной анафилаксии, сывороточной болезни, эндокардите, злокачественных опухолях, болезни Крона. Также циркулирующие иммунные комплексы исследуют в рамках общего иммунологического обследования.
Как регулируется иммунный ответ?
Защитная система организма отличается множеством механизмов контроля и регуляции протекающих в ней реакций. Это жизненно необходимо для любого сложного организма, так как если иммунный ответ будет слишком сильным – возникнут аутоиммунные заболевания и аллергии. При слишком слабой реакции – организм может не справиться с инфекцией либо ядом и получить фатальные повреждения.
Регуляция осуществляется на трех уровнях:
- Саморегуляция за счет внутренних механизмов взаимодействия иммунных клеток;
- Влияние гормональной системы и печени;
- Воздействие нервной системы.
Для саморегуляции в иммунной системе присутствуют специальные Т-хелперы, которые способны активировать либо подавлять производство антител. Также существуют особые клетки, которые производят антиидиотипы – особые белки связывающие собственные антитела, выработанные организмом ранее. Они нужны для своевременного снижения их концентрации, когда необходимость в большом количестве специфических иммуноглобулинов пропадает.
Гормональная система также играет большую роль в регуляции механизмов иммунного ответа. Практически все гормоны обладают способностью подавлять либо усиливать иммунные реакции. Например, гормон надпочечников гидрокортизон обладает мощным подавляющим действием на иммунный ответ. Поэтому препараты на его основе часто применяют для лечения аутоиммунных заболеваний.
Хорошим примером гормона – стимулятора иммунной системы является мелатонин (вырабатывается в шишковидной железе). Он оказывает мощное стимулирующее действие на иммунитет, но механизм его воздействия точно не установлен.
Печень является центром выработки различных иммуносупрессивных соединений. Играет важную роль в остановке активной фазы иммунного ответа, снижении активности лимфоцитов и макрофагов.
Активная роль центральной нервной системы в регуляции иммунного ответа давно известна. Осуществляют ее глубинные участки головного мозга, связанные с лимбической системой и отвечающие за психоэмоциональное состояние человека. Достоверно установлено, что депрессии и другие психические нарушения способны серьезно снижать активность защитной системы организма. Механизм регуляторного воздействия основан на передаче сигналов от нейронов непосредственно к клеткам иммунной системы.
Во многом параметры регуляции иммунной системы закладываются на генном уровне. У каждого человека закладывается индивидуальный набор генов, экспрессия которых в Т-хелперах обуславливает разную силу ответа у каждого индивидуума. За счет этого глубокого уровня регуляции природа создает большое разнообразие защитных реакций, что усложняет распространение инфекций в популяции.
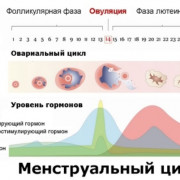
Схема Th1 ответа. Эффекторы клеточного ответа.
Пусковым звеном
в формировании клеточного типа иммунного
ответа является продукция макрофагом,
на территории которого идет процессинг
антигена, интерлейкина ИЛ-12. События
развиваются следующим образом.
ГКГС — I макрофага
презентирует пептид (антиген) Т-хелперу
(CD 4 ). Под влиянием ИЛ-12, продуцируемого
этим же макрофагом, Th трансформируется
в Th 1. g — IFN является важнейшим из цитокинов
, выделяемых Th 1. Он активирует контакт
Т CD 8 с рецептором ГКГС — I макрофага, на
котором представлен тот же антиген.
Выделяемый Th 1 ИЛ-2 стимулирует пролиферацию
таких, уже антигенспецифических
Т-цитолитических лимфоцитов (Тс). Главной
функцией Т с в противоинфекционной
защите является уничтожение соматических
клеток организма, внутри которых
находится возбудитель, а на поверхности
— метка, комплекс ГКГС-I — антиген патогена
. При прямом контакте с такой клеткой Т
с выделят гранулы, содержащие белки —
перфорин , гранзим . Перфорин встраивается
в мембрану соматической клетки, образует
в ней каналы «поры» и может действовать
как мембраноатакующий белок. Гранзим
( сериновые протеиназы ) индуцирует один
из вариантов апоптоза и гибель соматической
клетки вместе с находящимися в ней
микробами.
Выделяют три
основные группы Т- лимфоцитов- помощники
(активаторы), эффекторы, регуляторы.
Первая группа-
помощники (активаторы), в состав которых
входят Т- хелперы1, Т- хелперы2, индукторы
Т- хелперов, индукторы Т- супрессоров.
1. Т- хелперы1 несут
рецепторы CD4 (как и Т- хелперы2) и CD44,
отвечают за созревание Т- цитотоксических
лимфоцитов (Т- киллеров), активируют Т-
хелперы2 и цитотоксическую функцию
макрофагов, секретируют ИЛ-2, ИЛ-3 и другие
цитокины.
2. Т- хелперы2 имеют
общий для хелперов CD4 и специфический
CD28 рецепторы, обеспечивают пролиферацию
и дифференцировку В- лимфоцитов в
антителпродуцирующие (плазматические)
клетки, синтез антител, тормозят функцию
Т- хелперов1, секретируют ИЛ-4, ИЛ-5 и ИЛ-6.
3. Индукторы Т-
хелперов несут CD29, отвечают за экспрессию
антигенов HLA класса 2 на макрофагах и
других А- клетках.
4. Индукторы Т-
супрессоров несут CD45 специфический
рецептор, отвечают за секрецию ИЛ-1
макрофагами, активацию дифференцировки
предшественников Т- супрессоров.
Вторая группа- Т-
эффекторы. В нее входит только одна
субпопуляция.
5. Т- цитотоксические
лимфоциты (Т- киллеры). Имеют специфический
рецептор CD8, лизируют клетки- мишени,
несущие чужеродные антигены или
измененные аутоантигены (трансплантант,
опухоль, вирус и др.). ЦТЛ распознают
чужеродный эпитоп вирусного или
опухолевого антигена в комплексе с
молекулой класса 1 HLA в плазматической
мембране клетки- мишени.
Третья группа-
Т-клетки- регуляторы. Представлена двумя
основными субпопуляциями.
6
Т- супрессоры
имеют важное значение в регуляции
иммунитета, обеспечивая подавление
функций Т- хелперов 1 и 2, В- лимфоцитов.
Имеют рецепторы CD11, CD8. Группа функционально
разнородна
Их активация происходит в
результате непосредственной стимуляции
антигеном без существенного участия
главной системы гистосовместимости.
7. Т- контсупрессоры.
Не имеют CD4, CD8, имеют рецептор к особому
лейкину. Способствуют подавлению функций
Т- супрессоров, вырабатывают резистентность
Т- хелперов к эффекту Т- супрессоров.
Что выяснили российские учёные
Совсем недавно в авторитетном научном журнале Immunity исследование российских учёных на тему Т-клеток и коронавируса, в котором приняли участие 34 переболевших коронавирусом добровольца и две контрольные группы здоровых доноров.
«Действительно, не у всех переболевших коронавирусом обнаруживаются антитела. У части выздоровевших иммунный ответ обеспечивается только за счёт Т-клеток, чего, по всей видимости, оказывается достаточно», — объясняет Григорий Ефимов, заведующий лабораторией трансплантационной иммунологии Национального медицинского исследовательского центра (НМИЦ) гематологии Минздрава и один из авторов исследования.
Учёные также отметили, что ответ на фрагменты коронавируса есть не только у тех, кто им переболел, что может объясняться сезонными простудными заболеваниями в прошлом, которые были вызваны коронавирусами других типов. «При этом здоровые доноры, которых мы набирали во время пандемии, в среднем имели более высокий уровень ответа, чем те, образцы которых хранились в биобанке и были получены раньше. Скорее всего, это значит, что часть доноров имела контакт с вирусом, вызывающим COVID-19, не подозревая об этом», — добавляет Григорий Ефимов.
Иммунитет гуморальный
Полностью
разделить клеточный иммунитет и
гуморальный невозможно: в инициации
образованияантител участвуют
клетки, а в некоторых реакциях клеточного
иммунитета важную связующую функцию
выполняют антитела.
Гуморальный иммунный
ответ (образование антител) представляет
собой кульминацию ряда клеточных и
молекулярных взаимодействий, происходящих
в определенной последовательности:
— T-клетки
распознают антиген ,
представленный им антигенпрезентирующими
клетками ,
и в результате переходят в активированное
состояние;
— Tх-клетки ( хелперные
T-лимфоциты )
взаимодействуют с B-клетками, которые
презентируют им антигенные фрагменты;
— активированные
B-лимфоциты пролиферируют и дифференцируются
в антителообразующие клетки;
— начинается синтез
антител и от их класса зависит характер
последующего иммунного ответа.
28.Макрофаги (или
макрофагоциты) (от греч. makros — большой,
длинный, fagos — пожирающий) — это
гетерогенная специализированная
клеточная популяция защитной системы
организма.
Размер и форма
макрофагов варьируют в зависимости от
их функционального состояния. Обычно
макрофаги, за исключением некоторых их
видов, имеют одно ядро. Ядра макрофагов
небольшого размера, округлые, бобовидные
или неправильной формы. В них содержатся
крупные глыбки хроматина. Цитоплазма
базофильна, богата лизосомами, фагосомами
(что является их отличительным признаком)
и пиноцитозными пузырьками, содержит
умеренное количество митохондрий,
гранулярную эндоплазматическую сеть,
аппарат Гольджи, включения гликогена,
липидов и др.
В цитоплазме макрофагов выделяют т.н.
«клеточную периферию», обеспечивающую
макрофагу способность передвигаться,
втягивать микровыросты цитоплазмы,
осуществлять эндо- и экзоцитоз.
Непосредственно под плазмолеммой
находится сеть актиновых филаментов
диаметром 5—6 нм. Через эту сеть проходят
микротрубочки диаметром 20 нм, которые
прикрепляются к плазмолемме. Микротрубочки
идут радиально от клеточного центра к
периферии клетки и играют важную роль
во внутриклеточных перемещениях лизосом,
микропиноцитозных везикул и других
структур. На поверхности плазмолеммы
имеются рецепторы для опухолевых клеток
и эритроцитов, T- и B-лимфоцитов, антигенов,
иммуноглобулинов, гормонов. Наличие
рецепторов к иммуноглобулинам
обусловливает их участие в иммунных
реакциях.
Формы проявления
защитной функции макрофагов:
-
поглощение
и дальнейшее расщепление или изоляция
чужеродного материала; -
обезвреживание
его при непосредственном контакте; -
передача
информации о чужеродном материале
иммунокомпетентным клеткам, способным
его нейтрализовать; -
оказание
стимулирующего воздействия на другие
клеточные популяции защитной системы
организма.
Макрофаги имеют
органеллы, синтезирующие ферменты для
внутриклеточного и внеклеточного
расщепления чужеродного материала,
антибактериальные и другие биологически
активные вещества (например: протеазы,
кислые гидролазы, пироген, интерферон,
лизоцим и др.)
Количество макрофагов
и их активность особенно возрастают
при воспалительных процессах. Макрофаги
вырабатывают хемотаксические факторы
для лейкоцитов. Секретируемый макрофагами
IL-1 способен повышать адгезию лейкоцитов
к эндотелию, секрецию лизосомных
ферментов нейтрофилами и их цитотоксичность,
активирует синтез ДНК в лимфоцитах.
Макрофаги вырабатывают факторы,
активирующие выработку иммуноглобулинов
B-лимфоцитами, дифференцировку T- и
B-лимфоцитов; цитолитические
противоопухолевые факторы, а также
факторы роста, влияющие на размножение
и дифференцировку клеток собственной
популяции, стимулируют функцию
фибробластов.
Макрофаги
образуются из
стволовой клетки крови (СКК),
а также от промоноцита и моноцита крови
(т.е. имеют гематогенное происхождение).
Полное обновление макрофагов в рыхлой
волокнистой соединительной ткани
осуществляется примерно в 10 раз быстрее,
чем фибробластов.
Одной из разновидностей
макрофагов являются многоядерные
гигантские клетки, которые раньше
называли «гигантскими клетками инородных
тел», так как они могут формироваться,
в частности, в присутствии инородного
тела. Многоядерные гигантские клетки
представляют собой симпласты, содержащие
10—20 ядер и более, возникшие либо путем
слияния одноядерных макрофагов, либо
путем эндомитоза без цитотомии. По
данным электронной микроскопии, в
многоядерных гигантских клетках
присутствуют развитый синтетический
и секреторный аппарат и обилие лизосом.
Цитолемма образует многочисленные
складки.
Диагностика и результаты иммунологического анализа
Расшифровка иммунологического анализа крови состоит в интерпретации ряда цифр, обозначающих количество лейкоцитов, лимфоцитов и их популяций, моноцитов и другие показатели.
Иммуноглобулины (антитела) — это молекулы, находящиеся в крови и на поверхности слизистых оболочек, способные обезвреживать различные инфекционные возбудители и токсины, проникшие в организм.
Главной характеристикой антител является их специфичность, то есть каждый вид антител способен нейтрализовать только определенные вещества.

Известно пять классов иммуноглобулинов, три из них (А, М, G) наиболее изучены.
Расшифровка иммунологического анализа крови или иммунограмма дает полную картину состояния иммунитета конкретного человека.
В крови можно обнаружить 3 класса белков: А, М и G, по которым определяют, в какой стадии находится инфекционная болезнь (острой или хронической).
Иммунологический анализ направлен, в том числе, на их выявление.
Они позволяют определить стадию заболевания:
- А-глобулины появляются в первые 14 дней болезни;
- А и М-глобулины можно найти в крови со второй по третью неделю болезни;
- после 21 дня от начала заболевания в крови определяются все три типа;
- когда в крови пропали М-глобулины, а количество А и G снизилось более чем 2 раза, можно говорить о начале выздоровления;
- при хроническом процессе обязательно будет глобулин G, М отсутствует, А-глобулин может быть или не быть.
Расшифровка иммунологического анализа находится в компетенции врача-иммунолога, который даст заключение о состоянии иммунной системы.
Отклонение показателей в сторону уменьшения можно объяснить физическими нагрузками и стрессами, но если показатели увеличены, то это весьма тревожный симптом, который может стать поводом для проведения дополнительных исследований.
После расшифровки иммунологического анализа и постановки диагноза врач пропишет витамины или лекарственные средства, даст рекомендации по поводу режима дня и диеты.
Видео:
Для иммунологического анализа используют не саму кровь, а ее сыворотку, полученную в результате центрифугирования.
Перед сдачей крови на протяжении 12 часов нельзя ничего есть и пить, минимум час перед сдачей крови на иммунологический анализ нужно воздерживаться от курения, накануне нельзя принимать алкогольные напитки.
Итак, иммунологический анализ делают с целью определения количества в крови клеток, отвечающих за иммунитет, и иммунных комплексов.
Обследование предоставляет информацию о том, в каком состоянии находятся различные части иммунной защиты.
После получения результатов иммунологического анализа крови врач может скорректировать лечение, снизить или увеличить длительность приема антибиотиков, предвидеть появление аллергических реакций.
Видео:
https://youtube.com/watch?v=ptl6RXzma-U
16058
Типы иммунитета: какие есть?
Принято выделять два типа: индивидуальный, видовой. Последний присущ некоторому виду животных. Поскольку у человека тоже есть такое качество, нам не страшны патологии, опасные для некоторых форм жизни – скажем, собачья чумка. По аналогичной причине животным не страшны определенные заболевания, опасные (даже смертельно опасные) для человека. Видовой иммунитет обусловлен микроструктурным уровнем, он передается между поколениями внутри вида.
Индивидуальный тип иммунитета особь получает в течение своей жизни, не может передать по наследству. Такой формируется, если человек переживает инфицирование, отравление. Ряд болезней после себя дает стойкий иммунитет, при других патологиях его не наблюдается. В частности, если заболеть гонореей, иммунитет после выздоровления будет слабым, через короткое время полностью пропадает. При следующем контакте с возбудителем, вероятно, особь снова заболеет. А вот ветряная оспа, перенесенная однажды, оставляет после себя иммунитет на всю жизнь, поэтому болеть ею снова не придется.
Виды иммунного ответа
Все разновидности иммунных реакций можно разделить на две большие категории:
- Врожденные;
- Приобретенные.
Врожденный ответ обусловлен генетически закодированным механизмом защиты организма от патогенов. Это наиболее древняя система иммунитета, которая присутствует практически у всех живых организмов. Отличается быстрой реакцией и высокой эффективностью, токсин либо микроб уничтожается практически за считанные часы, что не приводит к развитию заболевания.
Некоторые исследователи относят к этой категории и противораковую активность иммунной системы. Но точные механизмы противоопухолевых реакций до конца не изучены. Нельзя исключить, что в итоге они будут выделены в отдельную категорию иммунного ответа.
Приобретенный иммунный ответ – возникает в ответ на попадание в организм патогенов, с которыми он ранее не встречался. Отличается многообразием проявлений, и различных симптомов. Например, кашель, насморк и повышение температуры тела во время простуды – внешние проявления сложных процессов, протекающих в иммунной системе, приводящих к уничтожению возбудителя.
За счет приобретенного иммунного ответа работают все вакцины, а также наступает естественное выздоровление от инфекционных заболеваний, отравлений токсинами, ядами животных.
Иммунный ответ также разделяют на клеточный и гуморальный. Такое деление несколько искусственное – в организме сложно отделить клеточные реакции от гуморальных, они тесно взаимосвязаны. Но оно позволяет упростить понимание этих сложных процессов.
Нюансы случая
Если иммунный ответ – это первичная реакция организма не встречу с вредоносной структурой, индуктивный этап по длительности в среднем недельный. Вторичная реакция обычно более быстрая – порядка трех суток или даже меньше. Это объясняется эффективностью клеточной памяти.

Иммунный ответ – это реакция взаимного влияния антигенпредставляющих клеточных структур, в медицине называемых макрофагами, и антигенов. Макрофаги могут экспрессировать детерминанты антигена на клеточной поверхности, тем самым получая данные о структуре и направляя ее на периферию иммунной системы. Именно в этой области генерируются Т-хелперы.
Другие факторы иммунитета
Каждый вид защиты организма от чужеродных агентов обладает своими, скажем так, исполнителями, которые стремятся уничтожить патогенное образование или хотя бы воспрепятствовать его проникновению в систему. Повторим, что иммунитет по одной из классификаций бывает:
1. Врожденный.
2. Приобретенный. Бывает активным (появляется после прививок и некоторых заболеваний) и пассивным (возникает в результате передачи антител младенцу от матери или введения сыворотки с готовыми антителами).
По другой классификации иммунитет бывает:
- Естественный (включает 1 и 2 типы защиты из предыдущей классификации).
- Искусственный (это тот же приобретенный иммунитет, появившийся после прививок или некоторых сывороток).
Врожденный тип защиты обладает следующими факторами:
- Механические (кожа, слизистые, лимфоузлы).
- Химические (пот, секреты сальных желез, молочная кислота).
- Самоочищение (слезы, шелушение, чихание и прочие).
- Антиадгезивные (муцин).
- Мобилизуемые (воспаление инфицированного участка, иммунный ответ).
Приобретенный тип защиты имеет только клеточные и гуморальные факторы иммунитета. Рассмотрим их подробнее.