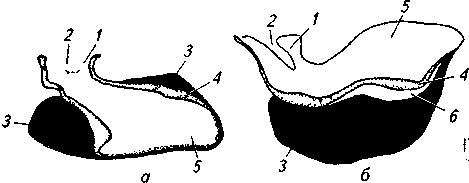
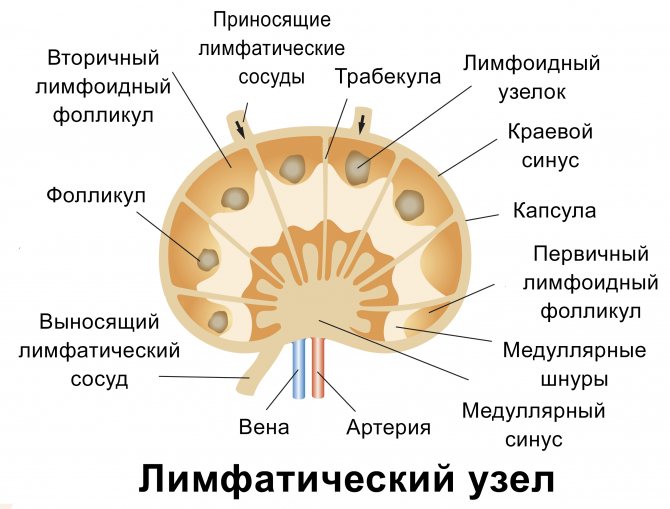
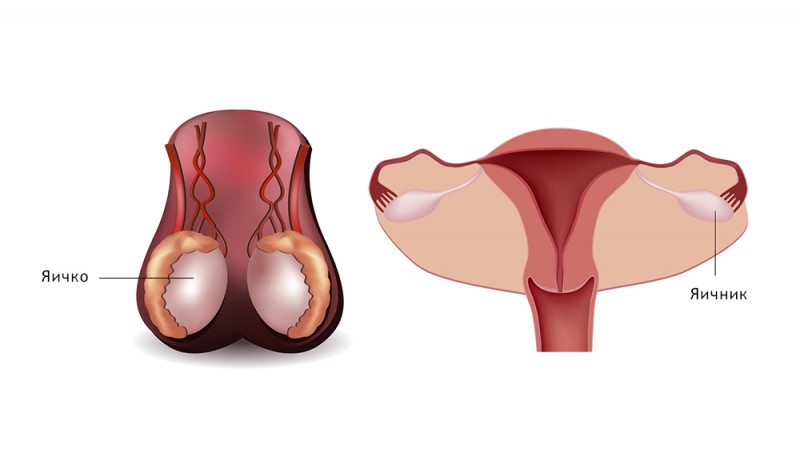
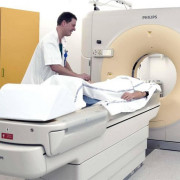
Периферические органы иммунной системы
Содержание:
- Особенности барьерной иммунной на разных уровнях
- Полезные методики для поддержания иммунитета
- Как повысить иммунитет
- Пониженный иммунитет: причины и симптомы
- Клетки иммунной системы
- Примечания[править | править код]
- Примечания[править | править код]
- Центральные органы иммунной системы
- Книги по укреплению иммунитета
- Клетки, участвующие в иммунном ответе
Особенности барьерной иммунной на разных уровнях
Строение мукозальной иммунной системы в разных частях организма достаточно сильно отличается. Это обусловлено специфическими условиями функционирования различных органов.
Дыхательный тракт
Основой барьерного иммунитета ЛОР-органов и дыхательных путей является глоточное кольцо. Оно состоит из нескольких скоплений лимфатической ткани:
- Глоточная миндалина;
- Язычная;
- Трубные миндалины;
- Небные.
Часть из них (небные, язычная) имеют в своем составе ветвящиеся углубления – крипты. Они значительно увеличивают площадь поверхности миндалин, являются основным местом взаимодействия иммуноглобулинов и других факторов барьерного иммунитета с микробами. Еще одна важная особенность этих органов – наибольшая концентрация В-лимфоцитов среди всех лимфоузлов.
Эти клетки вырабатывают IgA и G, которые выделяются в пространство крипт и на слизистую оболочку миндалин.
Еще один важный компонент барьерного иммунитета дыхательной системы – эпителиальный слой, который содержит множество иммунных клеток (Т и В лимфоциты, макрофаги). Такое строение сохраняется вплоть до нижних отделов легких. В них в эпителии начинают преобладать М-клетки и клетки, продуцирующие слизь. М-клетки выполняют важную функцию – транспортируют внутрь организма часть антигенов в неизменном виде. Это позволяет формировать «системный» ответ, что играют большую роль в формировании устойчивости ко многим заболеваниям.
Ротовая полость и ЖКТ
Полость рта выстилает многослойный эпителий, который выделяет большое количество слизи. Это препятствует развитию патогенных микробов. Слизь также содержит иммуноглобулины и другие факторы мукозального иммунитета.
Важной частью барьерной системы рта являются слюнные железы. Слюна содержит достаточно большие концентрации лизоцима, иммуноглобулинов и других веществ, которые связывают и подавляют развитие патогенных микроорганизмов
Нарушение состава либо выработки слюны является одним из основных факторов, приводящих к развитию кариеса, который вызван условно патогенными микробами, поселяющимися на эмали зуба.
Большую часть кишечника выстилает однослойный ворсинчатый эпителий. В его состав входят вырабатывающие слизь клетки, лимфоциты, М-клетки. Также большую роль в защите кишечника играют лимфатические скопления, к которым относят
- Пейеровы бляшки;
- Фолликулы толстой кишки;
- Аппендикс;
- Диффузная лимфоидная ткань в стенках желудка и пищевода.
Немаловажную роль играют, и симбиотические бактерии, обитающие преимущественно в толстом кишечнике. Это важный фактор иммунной защиты, без них нормальное функционирование пищеварительной системы и мукозального иммунитета было бы невозможным.
Урогенитальная систем
В целом функционирование барьерного иммунитета мочеполовых органов схоже с другими частями этой системы. Но есть ряд особенностей:
- Нет крупных лимфатических скоплений;
- Количество клеток иммунной системы ниже чем в других отделах;
- В составе слизи преобладают IgG, количество IgA невелико;
- Большое количество лактобацилл на поверхности эпителия.
Особенно много лактобактерий находится на поверхности эпителия влагалища. Именно они формируют кислую среду и выделяют ряд антибиотических веществ, которые препятствуют развитию патогенной микрофлоре в этом органе.
Кожа
Основа защитной системы кожных покровов – многослойный эпителий клетки которого при отмирании формируют практически непроницаемый защитный слой. На его поверхности обитает множество микроорганизмов (более 100 разновидностей). Они создают среду неблагоприятную для развития болезнетворных бактерий.
Дополнительными факторами защиты служат выделения сальных и потовых желез. Они содержат лизоцим, иммуноглобулины и другие защитные вещества.
Полезные методики для поддержания иммунитета
Для усиления защитных ресурсов медицина предлагает следующие решения:
- вакцинация, прививки;
- прием иммуностимулирующих медикаментов, витаминов;
- здоровый образ жизни.
Прививки делают новорожденным с первого месяца жизни. Далее проводится регулярная плановая вакцинация в возрасте 3-6 месяцев, в 1-3 года, в школьный период. Прививка позволяет внедрить в организм безопасные порции патогенов, чтобы спровоцировать «болезнь» в миниатюрном варианте, сохранив в памяти клеток механизм сопротивления. Сегодня есть немало противоборствующих позиций в обществе касательно целесообразности прививок. Но факты таковы, что миллионы детей избежали опасных заболеваний благодаря своевременной календарной вакцинации.
Прием витаминов и минералов, пищевых добавок и иммуностимуляторов – не гарантия стопроцентного здоровья. Однако шансы на успешное укрепление природной защитной функции существенно повышаются.
Есть жалобы на то, что иммунные препараты не демонстрируют должной эффективности. Но здесь снова не будет лишним вспомнить о сугубо индивидуальном характере приобретенного иммунитета. У каждого пациента эффективность от приема бывает разной. Далеко не всем подойдет тот или иной вариант, если он смог укрепить ресурсы одного человека.
Для профилактики инфекционных заражений можно заранее принять меры, которые достаточно действенны и помогают существенно улучшить состояние здоровья. Эти методы известны всем:
- регулярные занятия спортом;
- прогулки на свежем воздухе, в экологически чистых районах, парках, лесах;
- поездки на море, где соленый воздух и солнце заряжают наш организм большой порцией энергии (только не стоит злоупотреблять загаром);
- правильное, сбалансированное питание, прием витаминов.
Заголовок блока
Зачастую мы даже не замечаем микроскопических «болячек» и легкой простуды. Тело само справляется с задачей уничтожения опасности
Важно только своевременно выводить токсины и вести здоровый образ жизни для укрепления естественных иммунных сил
Как повысить иммунитет
Для укрепления защитных сил организма важно придерживаться сбалансированного питания. Рацион должен содержать все необходимые организму витамины и микроэлементы
Их лучше получать из натуральных продуктов. Чтобы иметь крепкий иммунитет, нужно соблюдать следующие рекомендации:
- Подготовиться к любой вспышке инфекционных заболеваний можно путем закаливания.
- Один из главных врагов иммунитета – стресс. Нужно научиться справляться с эмоциями.
- Полноценный сон, режим труда и отдыха обеспечат иммунную защиту.
- Укрепить организм поможет активный образ жизни. Эффективны аэробика, бег, плавание, длительные пешие прогулки.
- Отказ от вредных привычек, неконтролируемого потребления медикаментов поможет повысить иммунитет.
Пониженный иммунитет: причины и симптомы
С возрастом иммунитет способен снижаться. Это происходит под влиянием неблагоприятных факторов окружающей среды, вредных привычек, нездорового образа жизни. Ослабленный иммунитет уже не успевает отслеживать всех возбудителей заболеваний, проникших в организм, и своевременно убивать их. Так развиваются острые и хронические заболевания, ускоряются процессы старения.
К причинам, влияющим на снижение иммунитета, относят:
- Отсутствие режима дня, несоблюдение баланса между трудом и отдыхом, недостаток сна.
- Плохую экологию.
- Частые или длительные стрессы.
- Несбалансированное питание: скудный рацион, слишком жесткие диеты, голодания.
- Вредные привычки: злоупотребление кофе или алкоголем, курение.
- Недостаток витаминов и минералов.
- Злоупотребление медикаментозными препаратами (они оказывают на организм токсическое воздействие).
- Травмы, включая ожоги.
- Тяжелые физические нагрузки.
- Недавние операции.
Симптомами ослабленного иммунитета являются:
- Подверженность частым простудным заболеваниям (чаще 3 раз в год).
- Повышенная утомляемость.
- Нарушения сна, чувство усталости уже сразу после пробуждения.
- Вялость, слабость.
- Разбитое состояние.
- Герпесные высыпания.
- Частые воспалительные патологии полости рта (например, стоматит).
- Фурункулез.
- Субфебрильная (до 38 градусов) температура тела на протяжении долгого времени.
- Гнойные воспаления потовых желез.
- Частые и длительные (более 14 дней) обострения гайморита или бронхита.
- Нарушения функций ЖКТ.
- Инфекционные заболевания половых органов (микоплазмоз, хламидиоз, уреаплазмоз), лечение которых затруднено и растягивается на длительный период.
- Рецидивирующие и хронические патологии.
- Аллергические реакции, которых не было ранее.
- Аутоиммунные заболевания.
- Раковые опухоли.
Важно! При наличии симптомов снижения иммунитета необходимо обязательно обратиться к врачу. В противном случае могут развиться иммунодефицитные состояния (снижение активности гуморального и клеточного иммунитета)
Клетки иммунной системы
Иммунокомпетентными
клетками организма человека являются
Т– и В-лимфоциты.
T-лимфоциты
возникают в эмбриональном тимусе. В
постэмбриональном периоде после
созревания T-лимфоциты расселяются в
T-зонах периферической лимфоидной ткани.
После стимуляции (активации) определенным
антигеном T-лимфоциты преобразовываются
в большие трансформированные T-лимфоциты,
из которых затем возникает исполнительное
звено T-клеток.
Т-клетки
участвуют в:
1) клеточном
иммунитете;
2) регулировании
активности В-клеток;
3) гиперчувствительности
замедленного (IV) типа.
Различают
следующие субпопуляции Т-лимфоцитов:
1) Т-хелперы.
Запрограммированы индуцировать
размножение и дифференцировку клеток
других типов. Они индуцируют секрецию
антител В-лимфоцитами и стимулируют
моноциты, тучные клетки и предшественники
Т-киллеров к участию в клеточных иммунных
реакциях. Эта субпопуляция активируется
антигенами, ассоциируемыми с продуктами
генов МНС класса II – молекулами класса
II, представленными преимущественно на
поверхности В-клеток и макрофагов;
2) супрессорные
Т-клетки. Генетически запрограммированы
для супрессорной активности, отвечают
преимущественно на продукты генов МНС
класса I. Они связывают антиген и
секретируют факторы, инактивирующие
Т-хелперы;
3) Т-киллеры.
Узнают антиген в комплексе с собственными
МНС-молекулами класса I. Они секретируют
цитотоксические лимфокины.
Основная
функция В-лимфоцитов заключается в том,
что в ответ на антиген они способны
размножаться и дифференцироваться в
плазматические клетки, продуцирующие
антитела.
В-лимфоциты
разделяют на две субпопуляции: В1 и В2.
В1-лимфоциты
проходят первичную дифференцировку в
пейеровых бляшках, затем обнаруживаются
на поверхности серозных полостей. В
ходе гуморального иммунного ответа
способны превращаться в плазмоциты,
которые синтезируют только IgМ. Для их
превращения не всегда нужны Т-хелперы.
В2-лимфоциты
проходят дифференцировку в костном
мозге, затем в красной пульпе селезенки
и лимфоузлах. Их превращение в плазмоциты
идет с участием Т-хелперов. Такие
плазмоциты способны синтезировать все
классы Ig человека.
В-клетки
памяти – это долгоживущие В-лимфоциты,
произошедшие из зрелых В-клеток в
результате стимуляции антигеном при
участии Т-лимфоцитов. При повторной
стимуляции антигеном эти клетки
активируются гораздо легче, чем исходные
В-клетки. Они обеспечивают (при участии
Т-клеток) быстрый синтез большого
количества антител при повторном
проникновении антигена в организм.
Макрофаги
отличаются от лимфоцитов, но также
играют важную роль в иммунном ответе.
Они могут быть:
1) антигенобрабатывающими
клетками при возникновении ответа;
2) фагоцитами
в виде исполнительного звена.
Здоровье человека 24 часа в сутки находится под охраной. Море болезнетворных микробов сталкивается с нами круглосуточно: на улице, в транспорте, на учебе или работе, в магазинах и даже дома. Без надежной защиты этот мир не дал бы человеку шанса на существование. Поддержка приходит со стороны иммунитета, который каждую минуту несет верную службу, регулируя постоянство внутренней среды и не давая нежеланным элементам прорваться сквозь барьеры.
Примечания[править | править код]
- ↑ ИММУНИТЕТ • Большая российская энциклопедия — электронная версия. bigenc.ru. Дата обращения 8 апреля 2020.
- ↑ Bickle T. A., Krüger D. H. Biology of DNA restriction // Microbiological Reviews. — 1993. — Vol. 57, no. 7. — P. 434—450. — PMID 8336674.
- ↑ Черешнев В.А. Черешнева М.В. Иммунологические механизмы локального воспаления. Медицинская иммунология 2011 т.13 №6 стр.557-568 РО РААКИ. cyberleninka.ru. Дата обращения 16 мая 2020.
- ↑ Travis J. On the Origin of the Immune System // Science. — 2009. — Vol. 324, no. 5927. — P. 580—582. — doi:10.1126/science.324_580. — PMID 19407173.
- ↑ Genetics of the Immune Response / Ed. by E. Möller and G. Möller. — New York: Plenum Press, 2013. — viii + 316 p. — (Nobel Foundation Symposia, vol. 55). — ISBN 978-1-4684-4469-8. — P. 262.
- ↑ Галактионов В.Г. Проблемы эволюционной иммунологии. cyberleninka.ru. Медицинская иммунология 2004 т.6 №3-5 РО РААКИ. Дата обращения 16 мая 2020.
- ↑ Галактионов, 2005, с. 8.
- ↑ Галактионов, 2005, с. 8, 12.
- ↑ Иммунитет // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2.
- ↑ Нобелевская премия по физиологии и медицине 2011 (англ.). www.nobelprize.org.
- ↑ Галактионов, 2005, с. 392.
Примечания[править | править код]
- ↑ ИММУНИТЕТ • Большая российская энциклопедия — электронная версия. bigenc.ru. Дата обращения 8 апреля 2020.
- ↑ Bickle T. A., Krüger D. H. Biology of DNA restriction // Microbiological Reviews. — 1993. — Vol. 57, no. 7. — P. 434—450. — PMID 8336674.
- ↑ Черешнев В.А. Черешнева М.В. Иммунологические механизмы локального воспаления. Медицинская иммунология 2011 т.13 №6 стр.557-568 РО РААКИ. cyberleninka.ru. Дата обращения 16 мая 2020.
- ↑ Travis J. On the Origin of the Immune System // Science. — 2009. — Vol. 324, no. 5927. — P. 580—582. — doi:10.1126/science.324_580. — PMID 19407173.
- ↑ Genetics of the Immune Response / Ed. by E. Möller and G. Möller. — New York: Plenum Press, 2013. — viii + 316 p. — (Nobel Foundation Symposia, vol. 55). — ISBN 978-1-4684-4469-8. — P. 262.
- ↑ Галактионов В.Г. Проблемы эволюционной иммунологии. cyberleninka.ru. Медицинская иммунология 2004 т.6 №3-5 РО РААКИ. Дата обращения 16 мая 2020.
- ↑ Галактионов, 2005, с. 8.
- ↑ Галактионов, 2005, с. 8, 12.
- ↑ Иммунитет // Казахстан. Национальная энциклопедия. — Алматы: Қазақ энциклопедиясы, 2005. — Т. II. — ISBN 9965-9746-3-2.
- ↑ Нобелевская премия по физиологии и медицине 2011 (англ.). www.nobelprize.org.
- ↑ Галактионов, 2005, с. 392.
Центральные органы иммунной системы
Центральными
органами иммунной системы являются
костный
мозг и
вилочковая
железа (тимус).Это
органы
воспроизведения и селекции
клеток иммунной системы. Здесь происходит
лимфопоэз—
рождение, размножение
(пролиферация)
и дифференцировка
лимфоцитов
до стадии предшественников или зрелых
неиммунных (наивных) клеток, а также их
«обучение».
Внутри тела человека эти органы имеют
как бы центральное расположение.
У птиц
к центральным органам иммунной системы
относят сумку Фабрициуса (bursaFabricii),
локализованную
в области клоаки. В
этом органе происходит созревание и
размножение
популяции лимфоцитов — продуцентов
антител, вследствие чего они получили
название
В-лимфоциты
У
млекопитающих этого анатомического
образования
нет, и его функции в полной мере выполняет
костный мозг. Однако традиционное
название «В-лимфоциты» сохранилось.
Костный
мозглокализуется
в губчатом веществе костей
(эпифизы трубчатых костей, грудина,
ребра
и др.). В костном мозге находятся
полипотентные стволовые клетки, которые
являются родоначальницами
всех форменных элементов крови и,
соответственно, иммунокомпетентных
клеток. В
строме костного мозга происходит
дифференцировка и размножение
популяции
В-лимфоцитов,
которые затем разносятся по всему
организму кровотоком.
Здесь же образуются предшественники
лимфоцитов,
которые впоследствии мигрируют
в тимус, — это популяция Т-лимфоцитов.
Фагоциты
и некоторые дендритные клетки также
образуются
в костном мозге. В нем можно обнаружить
и плазматические
клетки.
Они образуются на
периферии в результате терминальной
дифференцировки
В-лимфоцитов, а затем мигрируют назад,
в костный мозг.
Вилочковая
железа, или
тимус,
или
зобная
железа,
располагается
в верхней части загрудинного
пространства. Этот
орган отличает особая динамика
морфогенеза. Тимус появляется в
период внутриутробного развития. К
моменту рождения
человека его масса составляет 10—15 г,
окончательно
он созревает к пятилетнему возрасту,
а максимального размера достигает к
10-12
годам жизни (масса 30—40 г). После периода
полового
созревания начинается инволюция органа
— происходит замещение лимфоидной
ткани
жировой и соединительной.
Тимус
имеет дольчатое строение. В его структуре
различают
мозговой и корковый слои.
В
строме коркового слоя
находится большое
количество эпителиальных клеток коры,
названных «клетки-няньки», которые
своими
отростками образуют мелкоячеистую
сеть, где располагаются «созревающие»
лимфоциты.
В пограничном, корково-мозговом слое
располагаются дендритные клетки тимуса,
а
в мозговом — эпителиальные клетки
Предшественники
Т-лимфоцитов, которые
образовались
из стволовой клетки в костноммозге,
поступают в корковый слой тимуса.
Здесь
под влиянием тимических факторов
они активно размножаются и дифференцируются
(превращаются) в зрелые Т-лимфоциты,
а
также
«учатся» распознавать чужеродные
антигенные
детерминанты.
Процесс
«обучения» состоит из двух этапов,
разделенных
по месту и времени, и
ивиочает
«положительную»
и
«отрицательнуюселекцию.
Положительная
селекция.
Суть ее заключается в «поддержке» клонов
Т-лимфоцитов,
рецепторы которых эффективно
связались с экспрессированными
на эпителиальных клетках собственными
молекулами
МНС, независимо от структуры
инкорпорированных
собственных олигопептидов.
Активировавшиеся в результате контакта
клетки получают от эпителиоцитов коры
сигнал на выживание и размножение
(ростовые
факторы тимуса), а нежизнеспособные или
ареактивные клетки погибают.
«Отрицательную»
селекциюосуществляют
дендритные
клетки в пограничной, корково-мозговой
зоне тимуса. Ее основная цель —
«выбраковка» аутореактивных клонов
Т-лимфоцитов.
Клетки, позитивно реагирующие на комплекс
МНС-аутологичный пептид, подвергаются
уничтожению путем индукции у них
апоптоза.
Итоги
селекционной работы в тимусе весьма
драматичны: более 99 % Т-лимфоцитов не
выдерживают
испытаний и погибают. Лишь менее
1 % клеток превращается в зрелые не-иммунные
формы, способные распознать в комплексе
с аутологичными МНС только чужеродные
биополимеры. Ежесуточно около 106
зрелых «обученных» Т-лимфоцитов покидают
тимус с крово- и лимфотоком и мигрируют
в различные органы и ткани.
Созревание
и «обучение» Т-лимфоцитов в тимусе
имеют важное значение для формирования
иммунитета. Отмечено, что эссенциальное
отсутствие или недоразвитие тимуса
ведет к резкому
снижению эффективности иммунной защиты
макроорганизма
Такое явление наблюдается
при врожденном дефекте развития
вилочковой
железы — аплазии или гипоплазии
Книги по укреплению иммунитета
Чтобы детально исследовать понятие иммунной системы и способы его укрепления, издаются тематические работы от известных авторов. Среди самых популярных:
- Умнякова Екатерина, «Как работает иммунитет»; 2018 год, издательство «Аванта». В книге Умняковой Е. излагается научное представление об иммунной системе, процессах в организме. Также автор развеивает устоявшиеся мифы, а с помощью простых аналогий и примеров из жизни доступно объясняет о всех процессах, связанных с иммунной системой человека.
- Фурман Джоэл, «Нетрадиционная медицина и народная кулинария»; 2013 год, издательство Эксмо. Недоспасов С. А., «Врожденный иммунитет и его механизмы»; 2012 год, издательство Научный мир.
Клетки, участвующие в иммунном ответе
T-Лимфоциты
Основная статья: T-лимфоцит
Субпопуляция лимфоцитов, отвечающая главным образом за клеточный иммунный ответ. Включает в себя субпопуляции Т-хелперов (дополнительно разделяются на Th1, Th2, а также выделяют Th3, Th9, Th17, Th22, Treg), цитотоксических Т-лимфоцитов, NKT. Включает в себя эффекторы, регуляторы и долгоживущие клетки-памяти. Функции разнообразны: как регуляторы и администраторы иммунного ответа (Т-хелперы), так и киллеры (цитотоксические Т-лимфоциты).
B-Лимфоциты
Основная статья: B-лимфоциты
Субпопуляция лимфоцитов синтезирующая антитела и отвечающая за гуморальный иммунный ответ.
Натуральные киллеры
Натуральные киллеры (NK-клетки) — субпопуляция лимфоцитов, обладающая цитотоксичной активностью, то есть они способны: контактировать с клетками-мишенями, секретировать токсичные для них белки, убивать их или отправлять в апоптоз. Натуральные киллеры распознают клетки, поражённые вирусами и опухолевые клетки.
Нейтрофилы
Нейтрофилы — это неделящиеся и короткоживущие клетки. Они составляют 95 % от гранулоцитов. Нейтрофилы содержат огромное количество антибиотических белков, которые содержатся в различных гранулах. К этим белкам относятся лизоцим (мурамидаза), липопероксидаза и другие антибиотические белки. Нейтрофилы способны самостоятельно мигрировать к месту нахождения антигена, так как у них есть рецепторы хемотаксиса (двигательная реакция на химическое вещество). Нейтрофилы способны «прилипать» к эндотелию сосудов и далее мигрировать через стенку к месту нахождения антигенов. Далее проходит фагический цикл, и нейтрофилы постепенно заполняются продуктами обмена. Далее они погибают и превращаются в клетки гноя.
Эозинофилы
Эозинофилы составляют 2—5 % от гранулоцитов. Способны фагоцитировать микробы и уничтожать их. Но это не является их главной функцией. Главным объектом эозинофилов являются гельминты. Эозинофилы узнают гельминтов и экзоцитируют в зону контакта вещества — перфорины. Эти белки встраиваются в билипидный слой клеток гельминта. В них образуются поры, внутрь клеток устремляется вода, и гельминт погибает от осмотического шока.
Базофилы
Базофилы составляют меньше, чем 0,2 % от гранулоцитов. Существуют две формы базофилов: собственно базофилы — базофилы, циркулирующие в крови и тучные клетки — базофилы, находящиеся в ткани. Тучные клетки располагаются в различных тканях, лёгких, слизистых и вдоль сосудов. Они способны вырабатывать вещества, стимулирующие анафилаксию (расширение сосудов, сокращение гладких мышц, сужение бронхов). При этом происходит взаимодействие с иммуноглобулином Е (IgE). Таким образом они участвуют в аллергических реакциях. В частности, в реакциях немедленного типа.
Моноциты
Моноциты превращаются в макрофаги при переходе из кровеносной системы в ткани, существуют несколько видов макрофагов в зависимости от типа ткани, в которой они находятся, в том числе:
- Некоторые антигенпредставляющие клетки, в первую очередь дендритные клетки, роль которых — поглощение микробов и «представление» их Т-лимфоцитам.
- Клетки Купфера — специализированные макрофаги печени, являющиеся частью ретикулоэндотелиальной системы.
- Альвеолярные макрофаги — специализированные макрофаги лёгких.
- Остеокласты — костные макрофаги, гигантские многоядерные клетки позвоночных животных, удаляющие костную ткань посредством растворения минеральной составляющей и разрушения коллагена.
- Микроглия — специализированный класс глиальных клеток центральной нервной системы, которые являются фагоцитами, уничтожающими инфекционные агенты и разрушающими нервные клетки.
- Кишечные макрофаги и т. д.
Функции их разнообразны и включают в себя фагоцитоз, взаимодействие с адаптивной иммунной системой и инициацию и поддержание иммунного ответа, поддержание и регулирование процесса воспаления, взаимодействие с нейтрофилами и привлечение их в очаг воспаления, выделение цитокинов, регуляция репарации, регуляция процессов свертывания крови и проницаемости капилляров в очаге воспаления, синтез компонентов системы комплемента.
Макрофаги, нейтрофилы, эозинофилы, базофилы и натуральные киллеры обеспечивают прохождение врождённого иммунного ответа, который является неспецифичным (в патологии неспецифичный ответ на альтерацию называют воспалением, воспаление является неспецифической фазой последующих специфических иммунных).