Новое поколение антибиотиков в таблетках: спектр применения
Содержание:
- Антибиотики какой фирмы лучше выбрать
- Номенклатура
- Фторхинолоны
- Основные группы антибиотиков и их представители, механизмы действия антибиотиков, антибиотики широкого спектра действия.
- Антибиотикорезистентность
- История
- Миф. Пероральные цефалоспорины такие же «сильные», как и парентеральные
- Роль антибиотиков в естественных микробиоценозах
- Почему алкоголь и антибиотики несовместимы?
- Таблица препаратов – антибиотиков
- Разделение препаратов по типу действия
- Номенклатура
- Терминология
- Место приложения действия.
- Совместимость фторхинолонов с другими антибиотиками
Антибиотики какой фирмы лучше выбрать
Нередко один и тот же препарат выпускают различные фармацевтические компании, поэтому их состав и дозировка могут незначительно отличаться. Врачи могут посоветовать пациенту, медикамент какого производителя купить, чтобы лечение прошло эффективнее. Лучшие антибиотики выпускают следующие фирмы:
- Astellas Pharma Europe – нидерландское представительство японской публичной компании, которая основана путем слияния 2-х фармацевтический фирм. В 1970-х годах они открыли свои офисы в Европе и США. В 2005 году произошло их объединение, штаб-квартиру разместили в Токио. Своей миссией компания видит улучшение здоровья людей за счет выпуска инновационных и надежных лекарств.
- KRKA – международная фармацевтическая компания, главный офис которой расположен в Словении. Основана в 1954 году как небольшая лаборатория. Выпускает препараты-дженерики. Их действующее вещество совпадает с оригиналом, но в составе присутствуют другие вспомогательные компоненты. Заводы фирмы расположены в Германии, Польше, России, Хорватии, Словении.
- Дальхимфарм – правопреемник Хабаровского Химзавода, который был основан в 1939 году. Его считают одним из старейших предприятий России по выпуску лекарств, входят в десятку ведущих фармпроизводителей страны. Основной принцип работы – предоставить клиентам эффективные, качественные и безопасные препараты. Вся продукция проверена московским центром контроля качества.
- Sandoz – фармацевтическая компания основана в Германии Эдуардом Сандозой и Альфредом Керном в 1886 году. Выпускает дженерики, которые используют при лечении различных заболеваний. Продукция представлена на рынках более 140 стран. Сейчас она входит в тройку лидеров производства амоксициллина.
- Laboratoires Bouchara-Recordati – основана в Италии в 1926 году. В 1999 и 2000 годах приобретает фармацевтические компании во Франции, на заводах которых начинает производство антибиотика фрамицетина под торговым названием Изофра. Продукция компании представлена на рынках Европы, США, Канады, Южной Америки, Северной Африки. Своей целью компания видит улучшение качества жизни людей.
- АО ФП «Оболенское» – российская фирма, создана на базе Государственного Научного Центра Прикладной Микробиологии в 1994 году. С 2013 года входит в группу компаний Алванса. Качество продукции, по результатам внешних аудитов, соответствует международным стандартам. Предприятие выпускает более 150 препаратов различных фармакотерапевтических групп. Среди них присутствуют дженерики и инновационные разработки.
- Pliva – самая крупная фармацевтическая компания в Южной Европе с главным офисом в г. Загреб, Хорватия. Основана в 1921 году, с 2008 года приобретена фирмой ТЕВА и действует как ее отдел. Основная деятельность направлена на разработку и производство дженериков. Самым популярным антибиотиком этой компании является Сумамед.
- GlaxoSmithKline – британская фармацевтическая фирма, основана в 2000 году путем слияния 2-х компаний. Представительства открыты в Германии, Италии, Австралии, Канаде, Польше и других странах. Основные заводы расположены в Сингапуре, США, Великобритании, Испании. Продукция представлена на рынках 160 стран. Популярным препаратом этой фирмы считают сильный антибиотик широкого спектра Аугментин.
- ПАО «Биосинтез» – группа компаний, в состав которой входят крупнейшие российские фармацевтические предприятия. Основана в Пензе в 1955 году. Первый антибиотик был выпущен в 1959 году. По выпуску препаратов-дженериков занимает 5 место в мире. Качество лекарств признано в 150 странах.
- OlainFarm – крупнейшая фармацевтическая компания стран Балтии, основана в 1972 году. Штаб-квартира расположена в Латвии. Качество продукции подтверждено аудитами известных фирм Швейцарии, США, Франции. На территории бывшего СССР компания стала первой, чей препарат внесен в список ВОЗ.
- Синтез – российский комбинат, был создан на базе Курганского завода медпрепаратов для производства антибиотиков. Также выпускает витамин В12 и эндокринные лекарства. С 1987 года инженеры внедрили новую технологию получения ампициллина тригидрата.
Номенклатура
Долгое время не существовало каких-либо единых принципов присвоения антибиотикам названий. Чаще всего их называли по родовому или видовому наименованию продуцента, реже — в соответствии с химическим строением. Некоторые антибиотики названы в соответствии с местностью, откуда был выделен продуцент, а, например, этамицин получил название от номера штамма (8).
В 1965 году Международный комитет по номенклатуре антибиотиков рекомендовал следующие правила:
- Если известна химическая структура антибиотика, название следует выбирать с учётом того класса соединений, к которому он относится.
- Если структура не известна, название даётся по наименованию рода, семейства или порядка (а если они использованы, то и вида), к которому принадлежит продуцент. Суффикс «мицин» присваивается только антибиотикам, синтезируемым бактериями порядка Actinomycetales.
- В названии можно давать указание на спектр или способ действия.
Фторхинолоны
Основные показания:
- Тяжелый наружный отит
- Синусит
- Обострение хронического бронхита
- Внебольничная пневмония
- Дизентерия
- Сальмонеллез
- Цистит, пиелонефрит
- Аднексит
- Хламидиоз и другие инфекции
Особенности:
мощные антибиотики, применяющиеся чаще всего при тяжело протекающих инфекциях. Могут нарушать формирование хрящей, в связи с чем противопоказаны детям и будущим мамам.
Наиболее частые побочные эффекты:
аллергические реакции, боли в сухожилиях, мышцах и суставах, боли и дискомфорт в животе, тошнота, диарея, сонливость, головокружение, повышение чувствительности к ультрафиолетовым лучам.
Основные противопоказания:
индивидуальная непереносимость, беременность, кормление грудью, возраст до 18 лет.
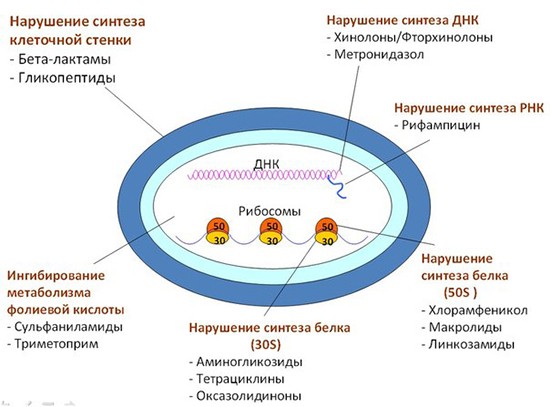
Основные группы антибиотиков и их представители, механизмы действия антибиотиков, антибиотики широкого спектра действия.
Антибиотики (противомикробные препараты)- это группа лекарственных препаратов, которые используются в лечении инфекционных заболеваний, вызванных бактериями, грибами и некоторыми другими микроорганизмами.
Антибиотиков либо препятствуют размножению бактерий и других микробов, либо приводят к их гибели.
Различают несколько основных групп антибиотиков, каждая из которых наиболее эффективна против определенных видов бактерий. Выбор того или иного антибиотика осуществляется врачом на основании предполагаемого возбудителя заболевания.
Как действуют антибиотики?
Антибиотики — это лекарства, выделенные из бактерий или грибов, используемые в лечении инфекционных заболеваний. С развитием науки, в арсенале врачей появились антибактериальные средства, полученные химическим путем, действующие так же, как и антибиотики.
Для удобства, мы будем называть антибиотиками и лекарства, полученные искусственным путем.
Различают 2 основных типа действия антибиотиков на бактерии: бактериостатический и бактерицидный.
Антибиотики с бактериостатическим эффектом не позволяют бактериям размножаться. Антибиотики с бактерицидным эффектом приводят к гибели бактерий.
Каждая группа антибиотиков эффективна против определенных типов бактерий, что связано с различными механизмами действия этих лекарств.
Ниже представлены наиболее распространенные группы антибиотиков, а также основные заболевания, при которых они применяются.
Антибиотикорезистентность
Антибиотикорезистентность принято делить на биологическую и клиническую. Под биологической антибиотикорезистентностью (антибиотикоустойчивостью) понимают способность микроорганизма противостоять действию антибиотика. Клиническая антибиотикоустойчивость — способность микроорганизмов выживать в присутствии концентраций антимикробного препарата, максимально достижимых в условиях данного организма.
Антибиотикорезистентность может быть как природной (в следствии отсутствия мишеней для антибиотика или невозможности ее достижения в микробной клетке), так и приобретенной. Примерами природной устойчивости может служить устойчивость к полимиксинам большинства Грамположительных микроорганизмов в силу недоступности мишени для полимиксинов (мембраны) из-за толстого муреинового слоя (грамположительной клеточной стенки). Другим примером природной устойчивости является природная устойчивость микобактерий к бета-лактамным препаратам в силу высокой гидрофобности клеточной стенки микобактерий.
Приобретенная антибиотикорезистентность возникает спонтанно вследствие мутаций и под воздействием антибиотика (или других индукторов мутаций) и закрепляется в популяции.
Механизмы резистентности
- У микроорганизма может отсутствовать структура, на которую действует антибиотик (например, бактерии рода микоплазма (лат. Mycoplasma) нечувствительны к пенициллину, так как не имеют клеточной стенки);
- Микроорганизм непроницаем для антибиотика (большинство грам-отрицательных бактерий невосприимчивы к пенициллину G, поскольку клеточная стенка защищена дополнительной мембраной);
- Микроорганизм в состоянии переводить антибиотик в неактивную форму (многие стафилококки (лат. Staphylococcus) содержат фермент β-лактамазу, который разрушает β-лактамовое кольцо большинства пенициллинов)
- Вследствие генных мутаций, обмен веществ микроорганизма может быть изменён таким образом, что блокируемые антибиотиком реакции больше не являются критичными для жизнедеятельности организма.
История
В 1928 году Александр Флеминг проводил рядовой эксперимент в ходе исследования болезнетворных бактерий. Вырастив колонии стафилококков, он обнаружил, что некоторые из них заражены обыкновенной плесенью Penicillium, которая растёт на лежалом хлебе, делая его зелёным. Вокруг каждой колонии плесени была область, в которой бактерий не было. Флеминг сделал вывод, что плесень вырабатывает вещество, убивающее бактерии, которое он назвал «пенициллин». Это и был первый современный антибиотик, о котором Флеминг доложил 13 сентября 1929 года на заседании Медицинского исследовательского клуба при Лондонском университете. Однако даже после опубликования статьи сообщение не вызвало у медиков энтузиазма. Дело в том, что пенициллин оказался очень нестойким веществом, он разрушался даже при кратковременном хранении.
Только в 1938 году двум учёным из Оксфордского университета, Говарду Флори и Эрнсту Чейну удалось выделить пенициллин в чистом виде. В связи с большими потребностями в медикаментах во время Второй мировой войны массовое производство этого лекарства началось уже в 1943 году. В 1945 году Флемингу, Флори и Чейну за их работу была присуждена Нобелевская премия.
В СССР первый советский антибактериальный препарат под названием «Крустозин» был получен советским микробиологом Зинаидой Ермольевой в 1942 году.
Изобретённый Ермольевой препарат в конце 40-х годов исследовали зарубежные учёные и пришли к выводу, что по своей эффективности он в 1,4 раза превосходит заокеанский пенициллин. Тогда Зинаида Ермольева и получила почётное имя — «Мадам Пенициллин».
Приблизительно с конца шестидесятых годов XX века до 2017 года фармакологи модифицировали уже известные препараты вслед за появлением резистентности бактерий к существующим, всё это время новые антибиотики не были найдены, и в мае 2017 года было объявлено о синтезе препарата, являющемся принципиально новым антибиотиком, а в 2018 году учёные объявили о создании нового класса антибиотиков на его основе.
Миф. Пероральные цефалоспорины такие же «сильные», как и парентеральные
Цефалоспорины (ЦС) — один из самых обширных классов антимикробных препаратов, представленных как в пероральной, так и парентеральной форме. При этом выраженность антибактериального эффекта в первую очередь определяется принадлежностью к одному из четырех поколений. Антибиотики цефалоспорины 1 поколения — парентеральный цефазолин и пероральный цефалексин — имеют самый узкий спектр активности, схожий со спектром аминопенициллинов (ампициллина, амоксициллина) . Цефалоспорины II поколения (парентеральный цефуроксим, пероральный цефаклор) активны в отношении грамотрицательных бактерий, при этом по действию на стафилококки и стрептококки они близки к предшественникам. Таким образом, мощность представителей антибиотиков первого и второго поколений практически не зависит от лекарственной формы. Но с цефалоспоринами последующих поколений всё не так просто.
Известно, что антибиотики 3 поколения обладают более высокой по сравнению с ЦС-I и ЦС-II активностью в отношении грамотрицательных бактерий, пневмококков и стрептококков. Однако их пероральные формы цефиксим и цефтибутен определенно обладают более узким спектром активности, чем парентеральные цефтриаксон, цефтазидим и цефоперазон. В частности, препараты для приема внутрь не действуют в отношении пенициллинорезистентных пневмококков, что связывают с их относительно невысокой биодоступностью. Так, биодоступность цефиксима составляет всего 40–50 %, в то время как у парентеральных форм она приближается к 100 % .
Тем не менее, цефиксим считается мощным антибиотиком, применение которого оправдано при инфекциях мочевыводящих путей, а также среднем отите и фарингите. Цефтибутен применяют гораздо реже: он показан только для терапии острых бактериальных осложнений хронического бронхита, среднего отита, фарингита и тонзиллита. Существенный недостаток этого препарата — низкая активность в отношении золотистого стафилококка . В то же время парентеральные цефалоспорины третьего поколения широко применяются для лечения тяжелых инфекций верхних, нижних дыхательных путей, желчевыводящих путей, мягких тканей, кишечных инфекций, сепсиса и других .
Роль антибиотиков в естественных микробиоценозах
Не ясно, насколько велика роль антибиотиков в конкурентных отношениях между микроорганизмами в естественных условиях. Зельман Ваксман полагал, что эта роль минимальна, антибиотики не образуются иначе как в чистых культурах на богатых средах. Впоследствии, однако, было обнаружено, что у многих продуцентов активность синтеза антибиотиков возрастает в присутствии других видов или же специфических продуктов их метаболизма. В 1978 году Л. М. Полянская на примере гелиомицина S. olivocinereus, обладающего свечением при воздействии УФ излучения, показала возможность синтеза антибиотиков в почвах. Предположительно особенно важны антибиотики в конкуренции за ресурсы среды для медленнорастущих актиномицетов. Было экспериментально показано, что при внесении в почву культур актиномицетов плотность популяции вида актиномицета, подвергающегося действию антагониста, падает быстрее и стабилизируется на более низком уровне, чем другие популяции.
Почему алкоголь и антибиотики несовместимы?
Известно три вида несовместимости между антибактериальными препаратами и алкоголем:
Дисульфирамподобные реакции. Некоторые антибиотики могут препятствовать разложению этилового спирта, на фоне чего в организме может накапливаться продукт, относящийся к неполному метаболизму, то есть уксусный альдегид. Именно это и провоцирует интоксикацию, проявляющуюся рвотой, и затрудненным дыханием. Похожим воздействием обладает препарат, который широко применяется для лечения алкоголизма, — «Дисульфирам», от него и пришло название данного типа взаимодействия. Не дают возможности алкоголю разлагаться нормально «Метронидазол» наряду с «Орнидазолом», «Тинидазолом» и цефалоспориновым антибиотиком «Цефотетаном». В том случае, если человек принимает какой-нибудь из данных препаратов, тогда спиртное полностью противопоказано. Специалистами рекомендуется воздерживаться от этанола в течение как минимум суток после завершения лечения «Метронидазолом». А также требуется три дня после терапии «Тинидазолом».
Нарушение функций метаболизма. Этиловый спирт, попадая в печень, как правило, разлагается под воздействием фермента цитохрома. Этот элемент принимает участие в метаболизме некоторых препаратов, к примеру, таких, как «Эритромицин», «Циметидин», противогрибковые лекарства («Вориконазол», «Итраконазол», «Кетоконазол»). В рамках одновременного поступления в печень алкоголя и препаратов, которые претендуют на свою долю цитохрома, неизбежно возникает конфликт. Часто проигравшей стороной оказывается лекарство. В организме возникает накопление препарата, что может привести к интоксикации.
Токсическое воздействие на нервную систему. Порой антибиотики несут специфические побочные эффекты, проявляющиеся сонливостью, седативным воздействием, головокружением. Известно всем и об успокаивающем эффекте алкоголя. Но одновременная комбинация двух седативных веществ в форме антибиотика и спиртного может угнетать нервную систему, что в особенности опасно для пожилых, водителей и так далее. К препаратам, которые угнетают ЦНС при совместном использовании со спиртным, относят «Циклосерин» наряду с «Этионамидом», «Талидомидом» и некоторыми другими. Так все серьезно, что нужно добавить в таблицу совместимости антибиотиков алкоголь. Последствия их употребления могут быть самыми печальными.
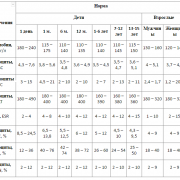
Таблица препаратов – антибиотиков
Классификация антибиотиков по группам, таблица распределяет некоторые виды антибактериальных препаратов в зависимости от химической структуры.
| Группа препаратов | Препараты | Сфера применения | Побочные эффекты |
| Пенициллин | Пенициллин. Аминопенициллин: aмпициллин, амоксициллин, бекaмпициллин. Полусинтетические: метициллин, оксациллин, клоксaциллин, диклоксациллин, флуклоксациллин. | Антибиотик с широким спектром воздействия. | Аллергические реакции |
| Цефалоспорин | 1 поколение: Цефалексин, цефадроксил, цепорин. 2: Цефамезин, цефуроксим (аксетил), цефазолин, цефаклор. 3: Цефотаксим, цефтриаксон, цефтизадим, цефтибутен, цефоперазон. 4: Цефпиром, цефепим. | Хирургические операции (для предотвращения осложнений), ЛОР-заболевания, гонорея, пиелонефрит. | Аллергические реакции |
| Макролиды | Эритромицин, рокситромицин, кларитромицин, азитромицин, азалиды и кетолиды. | ЛОР-органы, легкие, бронхи, инфекции органов малого таза. | Наименее токсичны, не вызывают аллергических реакций |
| Тетрациклин | Тетрациклин, окситетрациклин, хлортетрин, доксициклин, метациклин. | Бруцеллез, сибирская язва, туляремия, инфекции дыхательных и мочевыводящих органов. | Вызывает быстрое привыкание |
| Аминогликозиды | Стрептомицин, канамицин, амикацин, гентамицин, неомицин. | Лечение сепсиса, перитонитов, фурункулеза, эндокардита, пневмонии, бактериального поражения почек, инфекций мочевыводящих путей, воспаления внутреннего уха. | Высокая токсичность |
| Фторхинолоны | Левофлоксацин, гемифлоксацин, спарфлоксацин, моксифлоксацин. | Сальмонелла, гонококк, холера, хламидия, микоплазма, синегнойная палочка, менингококк, шигелла, легионелла, туберкулезная микобактерия. | Воздействуют на опорно-двигательный аппарат: суставы и кости. Противопоказаны детям и беременным женщинам. |
| Левомицетин | Левомицетин | Кишечные инфекции | Поражение костного мозга |
Основная классификация антибактериальных препаратов осуществляется в зависимости от их химической структуры.
Человеческий организм каждый день подвергается атаке множества микробов, которые стараются поселиться и развиваться за счет внутренних ресурсов тела. Иммунитет, как правило справляется с ними, но иногда устойчивость у микроорганизмов высокая и приходится принимать лекарства для борьбы с ними. Существуют разные группы антибиотиков, которые имеют определенный спектр воздействия, относятся к разным поколениям, но все виды этого препарата эффективно убивают патологические микроорганизмы. Как и все мощные медикаменты, это средство имеет свои побочные эффекты.
Разделение препаратов по типу действия
Как правило, чистые бактерицидные (уничтожающие возбудителя) и бактериостатические средства (подавляющие рост и размножение представителей патогенной флоры) не сочетают между собой. Это объясняется, в первую очередь, их механизмом действия. Бактерицидные препараты максимально эффективно действуют на организмы в стадии роста и размножения, поэтому применение бактериостатиков может стать причиной развития лекарственной устойчивости.
Важно понимать, что такое разделение по типу действия на бактерии не является абсолютным, и разные АБП могут давать различный эффект в зависимости от назначенной дозы. Например, увеличение суточной дозы или длительности применения бактериостатического средства, приводит к его бактерицидному действию
Например, увеличение суточной дозы или длительности применения бактериостатического средства, приводит к его бактерицидному действию.
Также, возможна избирательность действия на определённые возбудители. Будучи бактерицидными антибиотиками, пенициллины дают бактериостатический эффект против энтерококков.
Таблица совместимости антибиотиков по типу действия
| Бактерицидное | Бактериостатическое |
|
|
Сочетание антибиотиков между собой с учётом дозировки и типа действия на флору позволяет расширить спектр действия и увеличить эффективность проводимой терапии. Например, с целью предупреждения антибактериальной резистентности у синегнойной палочки возможно комбинирование антисинегнойных цефалоспоринов и карбапенемов, либо аминогликозидов с фторхинолонами.
- Рациональные комбинации антибиотиков для лечения энтерококков: дополнение пенициллинов аминогликозидами или применение триметоприма, в сочетании с сульфаметоксазолом.
- Расширенным спектром действия обладает комбинированный препарат второго поколения: Цифран СТ, сочетающий Ципрофлоксацин и Тинидазол.
- Эффективно сочетание цефалоспоринов и метронидазола. Тетрациклины комбинируют с гентамицином, для усиления действия на внутриклеточные возбудители.
- Аминогликозиды комбинируют с рифампицином, для усиления действия на серрации (часто рецидивирующие заболевания верхних дыхательных путей). Также комбинируются с цефалоспоринами, для повышения эффективности в отношении энтеробактерий.
Номенклатура
Долгое время не существовало каких-либо единых принципов присвоения антибиотикам названий. Чаще всего их называли по родовому или видовому наименованию продуцента, реже — в соответствии с химическим строением. Некоторые антибиотики названы в соответствии с местностью, откуда был выделен продуцент, а, например, этамицин получил название от номера штамма (8).
В 1965 году Международный комитет по номенклатуре антибиотиков рекомендовал следующие правила:
- Если известна химическая структура антибиотика, название следует выбирать с учётом того класса соединений, к которому он относится.
- Если структура не известна, название даётся по наименованию рода, семейства или порядка (а если они использованы, то и вида), к которому принадлежит продуцент. Суффикс «мицин» присваивается только антибиотикам, синтезируемым бактериями порядка Actinomycetales.
- В названии можно давать указание на спектр или способ действия.
Терминология
Полностью синтетические препараты, не имеющие природных аналогов и оказывающие сходное с антибиотиками подавляющее влияние на рост бактерий, традиционно было принято называть не антибиотиками, а антибактериальными химиопрепаратами. В частности, когда из антибактериальных химиопрепаратов известны были только сульфаниламиды, принято было говорить обо всём классе антибактериальных препаратов как об «антибиотиках и сульфаниламидах». Однако в последние десятилетия в связи с изобретением многих весьма сильных антибактериальных химиопрепаратов, в частности фторхинолонов, приближающихся или превышающих по активности «традиционные» антибиотики, понятие «антибиотик» стало размываться и расширяться и теперь часто употребляется не только по отношению к природным и полусинтетическим соединениям, но и ко многим сильным антибактериальным химиопрепаратам.
Место приложения действия.
Антибиотики отличаются друг от друга не только по химической структуре, но и по месту приложения действия на микробную клетку. Действие антибиотиков, применяемых в низких концентрациях, обычно направлено на специфические особенности жизнедеятельности патогенных микроорганизмов. Клеточные стенки бактерий и плесневых грибков сильно отличаются от клеточной оболочки животных клеток, и многие нетоксичные антибиотики блокируют образование именно клеточных стенок. Так действуют пенициллин, бацитрацин, циклосерин и цефалоспорины, применяемые в клинике при бактериальных инфекциях, а также гризеофульвин, который используется при кожных грибковых заболеваниях. Особо важную роль в жизнедеятельности бактериальной клетки играет ее плазматическая мембрана, расположенная под клеточной стенкой. Она регулирует прохождение в клетку питательных веществ и выход продуктов выделения, в ней протекают многие ферментативные процессы. Антибиотик полимиксин связывается с клеточной мембраной многих грамотрицательных бактерий и нарушает ее функцию. Тироцидин обладает химическими свойствами детергента и разрушает мембрану. На нее воздействует и стрептомицин: вновь синтезируемая мембрана оказывается дефектной, и клетка теряет жизненно важные для себя компоненты. Нистатин, связываясь с клеточными мембранами различных дрожжевых и плесневых грибков, приводит к потере их клетками необходимого элемента – калия. Во всех живых клетках происходит синтез белка. Хлорамфеникол специфически блокирует этот процесс у многих бактерий
Тетрациклины тоже блокируют белковый синтез, но не менее важной стороной их эффекта являются образование комплексов с металлами и влияние на связывание кальция, магния и марганца в клетке. На синтез белка воздействует также эритромицин
Изучение механизмов действия различных антибиотиков дало много полезных сведений о биохимических процессах, протекающих в клетках микроорганизмов. Даже те антибиотики, которые не применяются в лечебных целях, могут использоваться как важный инструмент биохимических исследований.
Основной механизм, посредством которого пенициллин убивает бактерии (в том числе культивируемые, что используется для определения чувствительности бактерий к антибиотику), в настоящее время хорошо изучен. Пенициллин действует на клеточную стенку бактерий; ее важнейшим компонентом являются пептидогликаны – сложные структуры, где сходные с глюкозой сахара связаны друг с другом поперечными пептидными мостиками, образованными аминокислотами. В норме пептидогликаны придают стенкам бактерий механическую прочность и устойчивость. Пенициллин так изменяет их биосинтез, что клеточная стенка теряет необходимую прочность. В результате содержимое бактериальной клетки вытекает, и клетка гибнет. Поскольку клетки млекопитающих имеют совершенно другую, не содержащую пептидогликанов, оболочку, пенициллин практически не действует на них. Таким образом, пенициллин, как правило, абсолютно безвреден для человека, если не считать редких побочных эффектов, например тяжелых аллергических реакций.
Совместимость фторхинолонов с другими антибиотиками
Также не указана в таблице совместимость фторхинолонов с другими антибиотиками. Поговорим об этом.
«Норфлоксацин», относящийся к фторхинолонам, нельзя одновременно сочетать с антацидами (в этом случае интервал между приемом должен составить более двух часов). Сочетание с нитрофуранами способно приводить к понижению антибактериальной активности. «Пефлоксацин» нельзя ни в коем случае разбавлять раствором натрия. В этой ситуации может повышаться действие непрямых антикоагулянтов наряду с концентрацией теофиллина в кровяной плазме.
Совместимость антибиотиков между собой должна учитываться в обязательном порядке.
«Ципрофлоксацин» повышает концентрацию «Теофиллина» в кровяной плазме. С точки зрения фармацевтики несовместимо это лекарство с растворами, которые имеют кислотность больше семи. Не стоит сочетать данный антибиотик с физически нестабильными растворами. В комбинации с «Варфарином» повышается концентрация последнего в крови