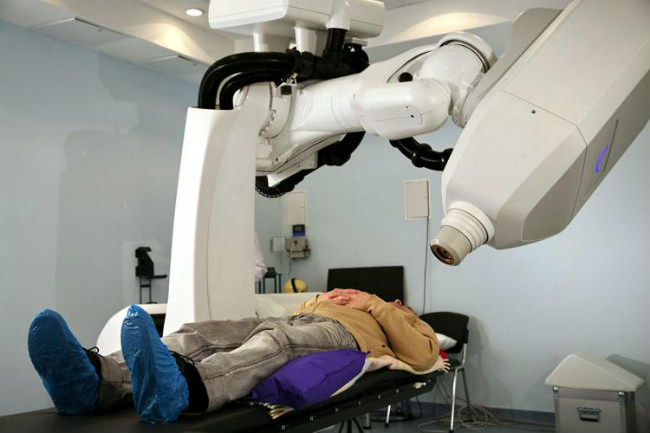
Лекарственная терапия
Содержание:
- Китруда/Keytruda (пембролизумаб)
- Кейтруда
- ФДТ при метастатическом поражении кожных покровов
- В каких случаях применяется иммунотерапия при раке молочной железы?
- Характеристика иммунотерапии
- Иммунотерапевтические препараты пассивного действия
- Опдиво
- Применение метода при лечении разных видов онкологии
- Адоптивная иммунотерапия рака
- Объясните, как это работает?
- Активная иммунотерапия
- Как проводится иммунотерапия аллергии
Китруда/Keytruda (пембролизумаб)
Препарат Китруда также является ингибитором контрольной точки. Он одобрен для лечения метастатического или неоперабельного рака, в клетках которого выявляется микросателлитная нестабильность (microsatellite instability, MSI), либо дефицит экспрессии одного или нескольких белков системы восстановления несоответствия ДНК (dMMR).
Имеются доказательства того, что Китруда может быть эффективна при лечении метастатического HER2-позитивного рака, когда препарат комбинируют с анти-HER2 таргетной терапией (например, с трастузумабом), если в опухоли присутствуют гиперэкспрессия PD-L1 и высокий уровень TILs (опухоль-инфильтрирующие лимфоциты).
Кейтруда
Кейтруда (другие названия: Пембролизумаб, MK-3475) — инновационный препарат, который был одобрен FDA (Американским управлением по надзору за качеством пищевых продуктов и медикаментов) в сентябре 2014 года, и в настоящее время уже достаточно широко применяется для лечения меланомы на поздних стадиях.
В 2014 году Кейтруда получила статус «приоритетное рассмотрение» и «прорыв в медицине». Это означает, что Пембролизумаб был включен в группу лекарственных средств, способных повысить эффективность и безопасность лечения редких и серьезных заболеваний. Именно поэтому препарат был так быстро одобрен и внедрен в клиническую практику. Обычно это происходит намного дольше.
Как действует Кейтруда?
Препараты для иммунотерапии меланомы и других злокачественных опухолей существуют уже достаточно давно. Но они всегда имели низкую эффективность, и до недавнего времени ученые не знали, как справиться с этой проблемой.
Задача иммунотерапии — активировать иммунную систему больного, заставить её атаковать и уничтожать раковые клетки. Долгое время препятствием для достижения этой цели становился белок PD-1. Это иммуноглобулин, молекулы которого встроены в клеточные мембраны. Он играет роль в дифференцировке иммунных клеток.
Белок PD-1 блокирует работу иммунной системы. Он не дает Т-лимфоцитам распознавать и уничтожать раковые клетки.
Кейтруда содержит моноклональные антитела, которые блокируют PD-1. Препарат помогает убрать «тормоз», благодаря чему лимфоциты приобретают способность атаковать опухолевую ткань.
Когда применяется этот препарат?
Показания к применению Кейтруды:
- метастазирующая меланома на поздних стадиях;
- неоперабельная меланома;
- отсутствие эффекта от лечения другими препаратами.
Насколько эффективна Кейтруда?
В Калифорнийском Университете в Лос-Анджелесе было проведено исследование, в котором приняли участие 173 человека с диагностированной прогрессирующей меланомой. Их разделили на две группы. В одной из них пациенты получали стандартную дозу препарата 2 мг на килограмм массы тела через каждые 3 недели. Во второй группе доза была увеличена в 5 раз (10 мг/кг).
У 24% пациентов, получавших препарат в дозе 2 мг/кг, опухоль уменьшилась более чем на треть. Повторный рост меланомы не отмечался, а эффект препарата сохранялся от 1,4 до 8,5 месяцев (в отдельных случаях — дольше).
Безопасна ли Кейтруда?
Второе исследование было проведено с участием 411 пациентов, которые имели прогрессирующую меланому и принимали Кейтруду. При этом тяжелые побочные эффекты со стороны кишечника, легких и печени отмечались редко.
Чаще всего у больных возникали такие побочные эффекты, как повышенная утомляемость, кашель, тошнота, сыпь, кожный зуд, снижение аппетита, запор, диарея, боли в суставах (источник данных об исследованиях — https://www.medicalnewstoday.com/articles/282101.php).
ФДТ при метастатическом поражении кожных покровов
Наряду с первичными и рецидивными злокачественными опухолями особое место занимает метастатическое поражение кожных покровов. По данным литературы, частота метастазов рака внутренних органов в кожу колеблется от 0,29 до 3,3%. Из метастатических злокачественных опухолей кожи наибольшую группу составляет рак молочной железы. Метастазы чаще локализуются на грудной стенке вблизи от первичной опухоли и преимущественно развиваются после хирургического лечения.
Основным методом лечения больных с внутрикожными метастазами рака молочной железы остается химио или гормонотерапия с многократным повторением курсов лечения. Второй по частоте причиной метастазов в кожу после рака молочной железы является меланома. Кожные и подкожные метастазы появляются примерно в 2-10% случаев. Метастазы могут быть единичные или множественные, располагаться вблизи первичного очага или отдаленно от него.
При лечении внутрикожных метастазов меланомы возможно применение хирургического лечения, лучевой терапии, комбинированного лечения. Однако при появлении новых очагов болезни в коже их применение становится сомнительным. Рост метастазов на фоне неэффективности традиционных методов лечения ухудшает прогноз жизни больных, способствует появлению впоследствии болевого синдрома, отека, интоксикации, что отрицательно сказывается на общем и психоэмоциональном состоянии больных, и снижения качества их жизни.
Именно такие пациенты нуждаются в лечении другими альтернативными методами, обладающими высокой противоопухолевой эффективностью. Одним из таких методов является ФДТ. Группой авторов проведена ФДТ с отечественными фотосенсибилизаторами у 36 пациентов с внутрикожными метастазами. При применении пролонгированной ФДТ у больных с внутрикожными метастазами рака молочной железы и меланомы полная регрессия опухолей получена в 39,3% и 38% соответственно, частичная – в 46% и 52,4%. У всех больных на фоне ранее проводимой традиционной терапии отмечена резистентность опухоли к традиционному лечению.
Таким образом, проведение ФДТ в значительной степени влияет на улучшение качества жизни этой сложной категории пациентов.
В каких случаях применяется иммунотерапия при раке молочной железы?
Моноклональные антитела применяют в случаях, когда рак является HER2-позитивным. Проверить это можно с помощью молекулярно-генетического анализа опухолевой ткани.
Иммунотерапия имеет некоторые преимущества перед химиотерапией:
- Она действует более прицельно, не повреждает здоровые клетки, и поэтому вызывает меньше побочных эффектов.
- Благодаря тому, что иммунопрепараты более безопасны, их можно вводить в течение длительного времени, применять в комбинациях с другими препаратами, не боясь усиления токсичности.
- Иммунная система может использовать в качестве мишеней разные антигены злокачественных опухолей, поэтому во время лечения у пациентов реже развивается резистентность.
Характеристика иммунотерапии
Иммунотерапия при онкологии: что это такое? Прежде всего иммунотерапия — это один из видов лекарственного лечения онкологических заболеваний наряду с химиотерапией, гормональной, таргетной, а также фотодинамической терапией. Причем восстановление иммунотерапевтическими препаратами, несмотря на свою относительную молодость, уже зарекомендовало себя как самостоятельный метод. Хотя, конечно, его применение в комбинации с другими методами на сегодняшний день также довольно распространено. Иммунотерапия не оказывает прямого влияния на опухоль — она воздействует непосредственно на иммунитет, повышая его и помогая ему справиться с заболеванием за счет активизации собственных (естественных) защитных ресурсов. Можно выделить несколько направлений действия иммунотерапии
- подавление роста и уничтожение раковых клеток;
- предупреждение рецидива онкологического заболевания и образования метастазов;
- снижение побочных эффектов иных видов лечения (например, лучевой терапии);
- нейтрализация осложнений, возникающих при опухоли в результате ослабления иммунитета.
Иммунотерапевтические препараты пассивного действия
Среди средств, которые также помогают бороться с опухолью — цитокины (интерфероны, интерлейкины, фактор некроза опухоли), моноклональные антитела, иммуностимулирующие средства.
Цитокины — это целая группа белков, которые регулируют взаимодействие между клетками иммунной, нервной, эндокринной систем. Они способы активировать иммунитет и потому применяются для иммунотерапии рака. К ним относят интерлейкины, белки интерфероны, фактор некроза опухолей и др.
Препараты на основе интерферона известны многим. С помощью одного из них многие из нас повышают иммунитет в период сезонных эпидемий гриппа, другими интерферонами лечат вирусные поражения шейки матки, цитомегаловирусную инфекцию и т. д. Эти белки способствуют тому, что клетки опухоли становятся «видимыми» для иммунной системы, распознаются как чужие по антигенному составу и удаляются собственными защитными механизмами.
Интерлейкины усиливают рост и активность клеток иммунной системы, которые элиминируют опухолевые элементы из организма больного. Они показали прекрасный эффект в лечении таких тяжелых форм онкологии как меланома с метастазами, метастазы рака других органов в почки.
Колониестимулирующие факторы активно используются современными онкологами и включены в схемы комбинированной терапии многих видов злокачественных опухолей. К ним относят филграстим, ленограстим.
Их назначают во время после или во время курсов интенсивной химиотерапии для повышения количества лейкоцитов и макрофагов в периферической крови больного, которые прогрессивно снижаются из-за токсического действия химиотерапевтических средств. Колониестимулирующие факторы снижают риск тяжелого иммунодефицита с нейтропенией и ряда сопутствующих им осложнений.
Иммуностимулирующие препараты повышают активность собственной иммунной системы пациента в борьбе с осложнениями, возникающими на фоне другого противоопухолевого интенсивного лечения, и способствуют нормализации формулы крови после облучения или химиотерапии. Они включены в состав комбинированного противоракового лечения.
Моноклональные антитела изготавливаются из определенных иммунных клеток и вводятся больному. Попав в кровяное русло, антитела соединяются со специальными чувствительными к ним молекулами (антигенами) на поверхности клеток опухоли, привлекают к ним цитокины и иммунные клетки самого пациента для атаки опухолевых. Моноклональные антитела могут быть «нагружены» лекарственными препаратами или радиоактивными элементами, которые фиксируются прямо на опухолевых клетках, вызывая их гибель.
Характер иммунотерапии зависит от разновидности опухоли. При раке почки может быть назначен ниволумаб. Метастатический почечный рак очень эффективно поддается лечению интерфероном альфа и интерлейкинами. Интерферон дает меньшее число побочных реакций, поэтому при раке почки он назначается чаще. Постепенный регресс раковой опухоли происходит на протяжении нескольких месяцев, в течение которых могут возникнуть такие побочные явления как гриппоподобный синдром, лихорадка, боли в мышцах.
При раке легкого могут быть использованы моноклональные антитела (авастин), противоопухолевые вакцины, Т-клетки, полученные из крови пациента и обработанные таким образом, чтобы появилась способность к активному распознаванию и уничтожению чужеродных элементов.
Препарат Кейтруда, активно применяющийся в Израиле и производимый США, показывает высочайшую эффективность при минимальных побочных эффектах. У принимавших его пациентов опухоль значительно уменьшалась или даже полностью исчезала из легких. Помимо высокой эффективности, препарат отличает и очень высокая стоимость, поэтому часть расходов на его приобретение в Израиле оплачивается государством.
Меланома — одна из самых злокачественных опухолей человека. В стадии метастазирования справиться с ней доступными методами практически невозможно, поэтому смертность все еще высока. Надежду на излечение или длительную ремиссию может дать иммунотерапия при меланоме, включающая назначение препаратов Кейтруда, ниволумаб (моноклональные антитела), тафинлар и других. Эти средства эффективны при запущенных, метастатических формах меланомы, при которых прогноз чрезвычайно неблагоприятен.
Опдиво
Опдиво (другое название — Ниволумаб) — препарат из группы моноклональных антител, одобренный FDA в конце декабря 2014 года.
В 2014 году этот препарат получил статусы: «принципиально новое лекарственное средство», «орфанный препарат», «ускоренное рассмотрение». Ниволумаб, так же, как и Кейтруда, был одобрен по ускоренной процедуре.
Как работает Опдиво?
По механизму действия препарат представляет собой аналог Кейтруды. Он блокирует рецептор PD-1, который снижает активность Т-лимфоцитов, не дает им распознавать и атаковать иммунные клетки.

В каких случаях планируется применять Ниволумаб?
Показания к применению препарата:
- прогрессирующая неоперабельная меланома;
- отсутствие эффекта от лечения Ипилимумабом;
- меланома, при которой имеется мутация гена BRAF, но применение ингибиторов BRAF не приносит эффекта.
Насколько эффективен Ниволумаб?
Эффективность Опдиво была изучена во время исследования, в котором приняли участие 120 больных с неоперабельной метастатической меланомой. В ходе применения препарата у 32% пациентов отмечалось существенное уменьшение размеров опухоли. Эффект сохранялся в течение 6 месяцев.
Безопасность
Также было проведено исследование, во время которого оценивалась безопасность препарата. 268 больных получали Ниволумаб, 120 — классическую химиотерапию.
Наиболее распространенные побочные эффекты, отмечавшиеся у больных, принимавших Опдиво: зуд, кожная сыпь, инфекции верхних дыхательных путей, кашель, задержка жидкости в организме (отеки).
Редко отмечаются тяжелые нарушения со стороны легких, толстой кишки, печени, почек и желез внутренней секреции. Эти побочные эффекты связаны с действием препарата на иммунитет (источник данных об исследованиях — https://www.medicalnewstoday.com/releases/287399.php).
Применение метода при лечении разных видов онкологии
Антигенспецифическая терапия активно используется врачами при онкологическом образовании в печени, коры головного мозга, пищевода, при глиобластоме. Применяется при опухоли в тканях мочевого пузыря, поджелудочной или предстательной железы, в районе шейки матки, груди, желудка и т.д. Врачи индивидуально подбирают курс терапии. На выбор лекарства влияет физическое состояние больного, медицинские показания, вид и стадия патологии.
Рак лёгких
Онкология в тканях лёгкого занимает одно из первых мест по диагностике. Мужчины страдают недугом чаще, чем женщины. Болезнь отличается высокой смертностью среди больных.
В организме присутствует небольшое количество раковых антигенов, на которые могут воздействовать иммунопрепараты. Это результативно используется в лечении заболевания. Особенно данный способ показывает высокую результативность во время диагностики немелкоклеточной онкологии, при мелкоклеточном раке лёгких процент выздоровления ниже.
В терапевтических мерах применяют перечисленные виды:
- Использование моноклональных антител для борьбы со злокачественным новообразованием;
- Применение ингибиторов, подавляющих защитные реакции организма;
- Назначение противоопухолевых препаратов;
- Клеточная стимуляция иммунитета, которая сопровождается лечебным перемещением Т-лимфоцитов.
В медицинской практике есть примеры появления побочных эффектов, поэтому терапия проходит в стационаре под контролем врача.
Рак молочной железы
Онкология молочной железы стоит на первых местах среди женских заболеваний злокачественного характера. Диагностируется в 12% всех патологий. При РМЖ повышается продуцирование белка-рецептора HER-2 – это приводит к стремительному делению злокачественных патогенов. Рак груди демонстрирует негативные онкологические свойства, заложенные на генетическом уровне.
Иммунотерапия применяется при наличии белка HER-2 в составе новообразования. Лекарство вводят в ткани опухоли при помощи тонкой иглы – это позволяет не травмировать здоровые ткани. Побочные эффекты при данном методе лечения практически не диагностируются, поэтому препараты можно использовать совместно с другими и в течение длительного периода времени.
У больной отмечается замедление роста опухоли, раковые клетки постепенно погибают. Женщина может прожить более 5 лет и вернуться к прежней жизни.
Другие виды онкологии
Онкологический процесс может начаться в любом органе – это зависит от многих факторов. Бывает рак простаты, кожи, крови и т.д. Опухоль в области головного мозга негативно влияет на зрение, память и координацию. Также наблюдаются другие тяжёлые симптомы, ухудшающие самочувствие человека. Определить болезнь на ранних сроках сложно из-за отсутствия выраженных признаков. Первые симптомы появляются при метастазах в другие органы тела.
Иммунотерапия применяется при следующих видах онкологии:
- При меланоме использование противоопухолевых антигенов помогает снизить показатели раковой интоксикации. Стимулирование работы защитных функций помогает остановить распространение меланомы по телу. В терапевтических целях применяют Кейтруда, Опдиво и другие.
- При онкологическом образовании в тканях желудка до 3 стадии используют хирургический метод лечения. Иммунотерапия требуется на последней неоперабельной стадии, чтобы приостановить распространение метастаз и купировать тяжёлые симптомы патологии. Применяют – Трастузумаб, Рамуцирумаб и т.п.
- При раке почек используют лекарственные препараты из группы цитокинов, ингибиторы контрольных точек.
Метод доказал результативность в лечении ряда болезней злокачественного характера. Выбор препарата зависит от вида опухоли и самочувствия больного.
Адоптивная иммунотерапия рака
Натуральные киллеры в отличие от других лимфоцитов способны эффективно лизировать (убивать) опухолевые клетки. Однако их численность невелика — всего 10-15 % всех лимфоцитов крови, что не позволяет им справиться с опухолевой массой. Чтобы увеличить количество лимфоцитов-киллеров, используется так называемая адоптивная (adoptive — привнесенный) иммунотерапия рака. Суть этих методов заключается в том, что из крови больного извлекают обыкновенные лимфоциты, затем в лабораторных условиях их обрабатывают особыми биологически активными веществами — так называемыми лимфокинами, полученными с использованием генно-инженерных технологий. Эти искусственно полученные вещества являются синтетическими аналогами естественных лимфокинов, синтезируемых в организме и участвующих в процессах регуляции и активации иммунитета.
Таким образом, адоптивная иммунотерапия рака позволяет из обычных лимфоцитов крови больного получить значительное количество так называемых лимфокинактивированных киллеров (ЛАК). Последние вводят в организм пациента, где они оказывают противоопухолевое действие.
ЛАК иммунотерапия рака расширяет спектр возможностей противоопухолевой терапии. Кроме того, она имеет ряд преимуществ по сравнению с химиотерапией и облучением: отсутствие токсичности и хорошая переносимость, возможность применения совместно с традиционными методами лечения, а также в случаях лекарственной резистентности, стимуляция местного противоопухолевого клеточного иммунитета, приводящая к лизису опухоли, улучшение качества и продолжительности жизни пациентов.
Адоптивная иммунотерапия рака с использованием ЛАК-клеток применяется главным образом для лечения так называемых иммуночувствительных форм злокачественных новообразований: меланомы и рака почки. В последние годы появились сведения о применении ЛАК-терапии и при других опухолях (раке легкого, яичников, желудка, при опухолевых плевритах и асцитах и т.д.).
В настоящее время практикуется иммунотерапия рака в адъювантном режиме, т.е. после радикальных операций, химио- и / или лучевого лечения, когда удается максимально уменьшить опухолевую массу. Это позволяет продлить продолжительность безрецидивного периода, улучшить качество жизни пациентов.
Иммунотерапия рака усиливает функциональную активность клеток иммунной системы организма с помощью цитокинов. Для этого у пациента берут кровь, из которой выделяют основные популяции лимфоцитов. При добавлении к ним в пробирке в стерильных условиях интерлейкина-2 и других биогенных веществ активность выделенных клеток возрастает по сравнению с исходной иногда в десятки раз. Вслед за этим активированные клетки, готовые к борьбе с опухолью, снова вводят пациенту.
Описанная иммунотерапия рака с использованием цитокинов и ЛАК-клеток направлена на стимуляцию неспецифического звена противоопухолевого иммунитета, однако нельзя оставлять без внимания то, что не задействованными в противоопухолевой защите остаются Т-киллеры, составляющие значительную часть популяции лимфоидных клеток и отвечающие за реализацию специфических иммунных механизмов. Поэтому в последнее время разрабатывают новые методы иммунотерапии, направленные на создание специфических противоопухолевых аутовакцин.
[], [], [], [], [], [], [], [], [], [], [], [], []
Объясните, как это работает?
Иммунотерапия мешает опухолевым клеткам сопротивляться иммунной системе. В норме иммунитет убивает все чужое или просто подозрительное, но опухолевые клетки умеют прикидываться «хорошими» либо «обманом» заставляют иммунитет отключаться.
На поверхности T-лимфоцитов (клеток иммунной системы) есть особые белки под кодовыми обозначениями PD-1 и CTLA-4. Их называют контрольными точками. Для иммунитета это как тормоза для машины. И опухолевые клетки умеют на них влиять, «жать на тормоза», чтобы иммунитет бездействовал. А иммунотерапевтические препараты могут эти тормоза отключать: T-лимфоцит «заводится» и атакует раковую клетку. Либо препарат блокирует другой белок (PD-L1), который скрывает опухоль от внимания иммунитета.
«T-клетка с помощью белка PD-1 связывается с белком PD-L1 здоровой клетки и понимает, что атаковать ее не нужно. Но некоторые опухолевые клетки тоже содержат белок PD-L1 — это позволяет им маскироваться под здоровые. Иммунотерапия влияет на иммунные клетки, как бы нейтрализуя белок PD-L1, и позволяет Т-клетке его игнорировать», — объясняет заведующий онкологическим отделением клиники «Медицина 24/7» Петр Сергеев.
Кроме того, в условиях лаборатории собственные Т-лимфоциты пациента можно «обучить» распознавать опухолевые клетки. Для этого Т-лимфоциты выделяют из крови пациента, а после «обучения» возвращают в организм, чтобы они находили и уничтожали опухолевые клетки. Такую разновидность иммунотерапии называют CAR-T, или Т-клеточная терапия. В прошлом году CAR-T стали применять в клиниках Великобритании.
Активная иммунотерапия
С
помощью вакцинации побеждены многие болезни, так почему бы не использовать эту
методику при карциноме в груди. Активная иммунотерапия при раке молочной железы
– это применение специальных вакцин, созданных из опухолевых клеток, взятых у
пациентки
Мы как бы говорим организму – вот, противоопухолевый иммунитет, посмотри,
обрати внимание, научись замечать, именно с этим ты должен бороться, именно это
ты должен победить
Еще
более прицельное воздействие – обучение лимфоцитов для борьбы с опухолью
(адоптивная клеточная терапия). Из крови пациентки забираются T-лимфоциты (киллеры), «натаскивают» их на раковые
клетки, выращивают будущих бойцов с опухолью и возвращают в кровь.
Пока все это на уровне клинических исследований,
которые проводятся в крупных медицинских центрах. До массового использования
еще далеко, но – есть надежда, что эти методики в будущем помогут побежать карциному.
Как проводится иммунотерапия аллергии
Иммунотерапия аллергеном может проводиться перорально или подкожно. Еще одно подразделение десенсибилизации зависит от продолжительности действия аллергенов. Предсезонная десенсибилизация применяется у людей с аллергией на сезонные аллергены, круглогодичная десенсибилизация – у людей с аллергией на аллергены, возникающей круглый год. Схема десенсибилизации к сезонным и многолетним аллергенам очень похожа, отличается только время начала терапии.
Аллергенная иммунотерапия в случае аллергии на аллергены, возникающей в течение года (например, на клещей домашней пыли), может быть начата в любое время, независимо от времени года. Терапия сезонных аллергенов может проводиться в предсезонной системе. Для пыльцы растений десенсибилизация начинается в осенне-зимний период и прекращается во время воздействия аллергенов, то есть в сезон пыльцы, или круглогодично — меньшие дозы аллергена вводятся в течение всего года.
Тип используемой иммунотерапии выбирается лечащим врачом на основании предыдущего собеседования и результатов анализов.
Лечение проходит в два этапа. Первый — врач вводит пациенту все более высокие дозы аллергена, пока не будет достигнут максимум. Затем пациент получает эту дозу во второй части лечения.
На практике это выглядит так:
- Первая фаза. В течение первых трех месяцев круглогодичной десенсибилизации вакцины вводятся с интервалом в 7–14 дней. Дозы вводимого аллергена постепенно увеличиваются до достижения максимального значения концентрации;
- Поддерживающая фаза. Постоянная поддерживающая доза аллергена вводится каждые 4-6 недель, а вся терапия длится от 3 до 5 лет в зависимости от чувствительности организма.
Схема предсезонной иммунотерапии немного отличается, в основном из-за более короткого времени десенсибилизации. В безаллергенный период пациенту вводят до десятка доз аллергена каждые 7-14 дней.
На успех десенсибилизации влияют внешняя среда и решения врача и пациента
Первое важное решение — это правильный выбор вакцины для пациента, т.е. какой тип аллергена и терапию выбрать
По этой причине необходимы диагностика и тщательное интервью с пациентом.
Из-за специфики десенсибилизации важно максимально устранить аллерген из окружающей среды. Независимо от используемой вакцины, десенсибилизацию лучше всего начинать при минимальном воздействии аллергенного фактора, то есть при:
- аллергии на пыльцу растений – в осенне-зимний период,
- круглогодичной аллергии – в момент наименьшей выраженности симптомов.
Только вакцины, принимаемые систематически и через определенные промежутки времени, гарантируют эффективность иммунотерапии, поэтому пациент обязан посещать кабинет аллерголога в среднем один раз в месяц. Тогда первые эффекты лечения будут видны через год терапии.
Прием аллерголога
К сожалению, иммунотерапия может быть неэффективной у людей, страдающих острой астмой и атопическим дерматитом.