Острый миелобластный лейкоз: причины, первые симптомы, как лечить патологию
Содержание:
- Признаки, симптомы, проявления
- Симптомы Хронического миелоидного лейкоза:
- Ссылки
- Особенности питания
- Симптомы Острого миелоидного лейкоза (острого нелимфобластного лейкоза, острого миелогенного лейкоза):
- Происхождение[править | править код]
- Хронический миелолейкоз
- Диета
- Расположение в организме[править | править код]
- Острый миелобластный лейкоз – что это такое?
- Как продлить срок жизни
- Диагностика ОМЛ
- Выживаемость
Признаки, симптомы, проявления
Клиническая картина заболевания складывается из ряда синдромов:
- Анемический синдром. Характерны бледность кожных покровов, ощущение слабости, головокружение, сердцебиение, одышка. В анализе крови отмечают снижение уровня гемоглобина (для женщин – ниже 120 г/л, для мужчин – менее 130 г/л), уменьшение красных кровяных телец (эритропения), повышение СОЭ.
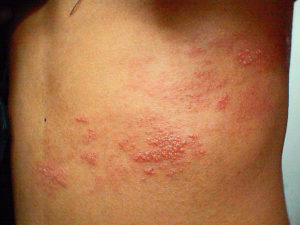
- Геморрагический синдром. Связан с нарушением производства тромбоцитов. Он отличается повышенной кровоточивостью, на кожных покровах возникают петехии (кровоизлияния малых размеров), геморрагии, возможно образование кровоизлияний. В клиническом анализе крови наблюдают снижение тромбоцитов менее 150 тысяч в микролитре (тромбоцитопения).
- Гиперпластический синдром. Характеризуется увеличением лимфатических узлов (безболезненны, не спаяны с кожей, подвижны), увеличением размеров печени и селезенки. Пациенты предъявляют жалобы на болезненность в области костей, в особенности позвоночника и нижних конечностей. Снижаются показатели лимфоцитов, лейкоцитов. Появляются патологически измененные лейкоцитарные клетки.
- Интоксикационный синдром. Проявляется лихорадочной реакцией (повышением температуры тела до индивидуально высоких цифр), вялостью, апатией, цефалгией, ознобом, миалгиями.
- Синдром инфекционных осложнений. Связан с нарушением иммунного статуса организма. Понижается его резистентность к различным инфекциям, способность самостоятельно с бороться с ними. Часто заболевания вызываются флорой, которая является нормальной для организма человека. Зачастую происходит присоединение грибковой инфекции (кандидоз).
Симптомы Хронического миелоидного лейкоза:
Момент возникновения хронического миелоидного лейкоза, как и любого другого лейкоза, не имеет симптомов и всегда проходит незамеченным. Симптоматика развивается тогда, когда общее количество опухолевых клеток начинает превышать 1 килограмм. Большинство пациентов жалуются на общее недомогание. Они быстрее устают, и при физической работе у них может возникать одышка. В результате анемии кожа становится бледной. Пациенты могут испытывать дискомфорт в левой половине брюшной полости, вызванный увеличением селезенки. Нередко пациенты теряют в весе, отмечают усиленную потливость, похудание и неспособность переносить жару. При клиническом осмотре чаще всего единственным патологическим признаком является увеличение селезенки. Увеличения размеров печени и лимфатических узлов в ранней стадии ХМЛ практически не встречается. Примерно у четверти заболевших хронический миелоидный лейкоз обнаруживают совершенно случайно, во время планового медицинского обследования. Иногда диагноз ХМЛ ставится уже на более агрессивной стадии — акселерации или бластного криза.
Хронический миелоидный лейкоз (хронический миелоз) протекает в две стадии.
Первая стадия — доброкачественная, длится несколько лет, характеризуется увеличением селезенки.
Вторая стадия — злокачественная, длится 3-6 месяцев. Селезенка, печень, лимфатические узлы увеличены, появляются лейкозные инфильтрации кожи, нервных стволов, мозговых оболочек. Развивается геморрагический синдром.
Часто регистрируются инфекционные заболевания. Типичны признаки интоксикации — слабость, потливость. Иногда первым симптомом является небольшая боль, тяжесть в левом подреберье, что связано с увеличением селезенки, в последующем бывают инфаркты селезенки. Без видимой причины поднимается температура, появляются боли в костях.
В типичном случае характерен нейтрофильный лейкоцитоз (повышение уровня нейтрофильных лейкоцитов) с появлением молодых форм нейтрофилов, сопровождающийся увеличением количества тромбоцитов, уменьшением содержания лимфоцитов. По мере развития болезни нарастают анемия и тромбоцитопения. У детей чаще наблюдается ювенильная форма хронического миелолейкоза без увеличения количества тромбоцитов, но с повышенным содержанием моноцитов. Часто увеличивается число базофилов, имеет место повышенный уровень эозинофилов. В первую доброкачественную стадию клетки костного мозга по всем параметрам соответствуют норме. Во вторую стадию в костном мозге и крови появляются бластные формы, отмечается быстрый рост числа лейкоцитов в крови (до нескольких миллионов в 1 мкл). Характерными признаками конечной стадии является обнаружение в крови осколков ядер мегакариоцитов, угнетение нормального кроветворения.
Болезнь протекает хронически с периодами обострения и ремиссиями. Средняя продолжительность жизни — 3-5 лет, но известны отдельные случаи длительного течения хронического миелолейкоза (до 10-20 лет). Клиническая картина зависит от стадии заболевания.
Прогноз неоднозначен и зависит от стадии заболевания. В течение первых двух лет после постановки диагноза умирают 10% больных, каждый последующий год — чуть меньше 20%. Медиана выживаемости составляет примерно 4 года.
Для определения стадии заболевания и риска летального исхода используют прогностические модели. Чаще всего это модели, основанные на многофакторном анализе наиболее важных прогностических признаков. Одна из них — индекс Сокала — учитывает процент бластных клеток в крови, размеры селезенки, число тромбоцитов, дополнительные цитогенетические нарушения и возраст. В модели Тура и комбинированной модели Кантарджана учитывается число неблагоприятных прогностических признаков. К таким признакам относятся: возраст 60 лет и старше; значительная спленомегалия (нижний полюс селезенки выступает из левого подреберья на 10 см или более); содержание бластных клеток в крови или в костном мозге, равное или превышающее 3% и 5% соответственно; содержание базофилов в крови или в костном мозге, равное или превышающее 7% и 3% соответственно; уровень тромбоцитов, равный или превышающий 700000 1/мкл, а также все признаки стадии ускорения. При наличии перечисленных признаков прогноз крайне неблагоприятный; риск летального исхода в течение первого года заболевания втрое больше обычного.
Ссылки
- Wilson J.D., Braunwald E., Isselbacher K.J., Martin J.B., Fauci A.S., Root R.K. Harrison’s Principles of Internal Medicine 12th edition. McGraw-Hill Inc.(1991).
- Curran R.C., Crocker J. Curran’s Atlas of Histopathology 4th edition. Harvey Miller Publishers LTD. Oxford University Press Inc.(distributor).(2000).
- Bloom W., Fawcett D.W. A Textbook of Histology 12th edition. W.B. Saunders Company
- Murohashi I., Tohda S., Suzuki T., Nagata K., Yamashita Y., Nara N.(1989).Autocrine growth mechanisms of the progenitors of blast cells in acute myeloblastic leukemia. Journal of the American Society of Hematology 74, 35-41
- Villamor N., Zarco M-A., Rozman M., Ribera J-M., Feliu E., Montserrat E.(1998).Acute myeloblastic leukemia with minimal myeloid differentiation: phenotypical and ultrastructural characteristics. Leukemia 12, 1071—1075
- News and views.(1949).Journal of the American Society of Hematology 4, 89-96
- Williams Majorie J.(1955).Myeloblastic Leukemia Preceded by Prolonged Hematologic Disorder. Journal of the American society of hematology 10, 502—509
- Beutler E.,Lichtman M.,Coller B.,Kipps T. Williams Hematology 5th edition. McGraw-Hill Inc.(1995).
Особенности питания
Несмотря на ухудшение аппетита, наблюдающееся при хроническом и остром миелоидном лейкозе, необходимо придерживаться предписанного специалистом режима питания.
Для восстановления сил, удовлетворения потребностей организма, угнетенного миелобластным (миелоидным) лейкозом, предотвращения неблагоприятных последствий интенсивной терапии белокровия, необходима сбалансированная диета.
При миелолейкозе и других формах лейкемии рекомендуется дополнять рацион питания:
- Продуктами, богатыми витамином C, микроэлементами.
- Зеленью, овощами, ягодами.
- Рисовой, гречневой, пшеничной кашей.
- Морской рыбой.
- Молочными продуктами (нежирным пастеризованным молоком, творогом).
- Мясом кролика, субпродуктами (почками, языком, печенью).
- Прополисом, медом.
- Травяным, зелёным чаем (оказывает антиоксидантное действие).
- Оливковым маслом.

Для недопущения перегрузок пищеварительного тракта и других систем при миелолейкозе из меню исключают:
- Алкоголь.
- Продукты, содержащие трансжиры.
- Фастфуд.
- Копчёные, жареные, изобилующие солью блюда.
- Кофе.
- Сдобу, кондитерские изделия.
- Продукты, способствующие разжижению крови (лимон, калину, клюкву, какао, чеснок, орегано, имбирь, паприку, карри).
При миелолейкозе необходимо контролировать объём потребления белковой пищи (не более 2 г. в сутки на 1 кг. массы тела), поддерживать водный баланс (от 2-2,5 л. жидкости в сутки).
Симптомы Острого миелоидного лейкоза (острого нелимфобластного лейкоза, острого миелогенного лейкоза):
Клиническая картина ОМЛ достаточно хорошо известна и проявляется следующими синдромами: анемическим, геморрагическим и токсическим, которые характеризуются бледностью кожных покровов, выраженной слабостью, головокружением, снижением аппетита, повышенной утомляемостью, лихорадкой без проявлений катаральных явлений.
Лимфатические узлы у большинства больных — небольших размеров, безболезненные, не спаяны с кожей и друг с другом. В редких случаях наблюдаются увеличенные лимфатические узлы размером от 2,5 до 5 см с образованием конгломератов в шейно-надключичной области. Изменения в костно-суставной системе в некоторых случаях проявляются выраженными оссалгиями в нижних конечностях и в области позвоночного столба, что сопровождается нарушением движений и походки. На рентгенограммах костной системы отмечаются деструктивные изменения различной локализации, периостальные реакции, явления остеопороза. У большинства детей наблюдается небольшое увеличение печени и селезенки (выступают из-под края реберной дуги на 2-3 см).
Экстрамедуллярные опухолевые поражения чаще проявляются гингивитом и экзофтальмом, в том числе двусторонним; в редких случаях бывают опухолевая инфильтрация мягких тканей, гипертрофия нёбных миндалин, поражение носоглотки и лицевого нерва, а также лейкемиды на коже.
Экстрамедуллярные локализации ОМЛ объединяет термин «гранулоцитарная (миелобластная) саркома», включающая классическую хлорому и непигментированные опухоли.
По данным аутопсии, гранулоцитарная (миелобластная) саркома диагностируется в 3-8% случаев у больных ОМЛ. Она может предшествовать или сочетаться с признаками ОМЛ, характеризующимися бластной инфильтрацией костного мозга и наличием бластов в периферической крови, а также наблюдаться при рецидиве заболевания. Наиболее частой локализацией опухолевого роста является орбита (поражаются орбитальная ткань и внутренние структуры черепа). Бластные клетки чаще представлены М2-типом, имеющими транслокацию t(8;21). Ряд авторов указывают на более плохой прогноз у этих больных, чем при типичном ОМЛ.
Факторы прогноза у больных ОМЛ менее изучены, чем у больных с ОЛЛ. Было проведено большое количество одно- и многофакторных исследований, с помощью которых появилась возможность определения благоприятных и неблагоприятных признаков заболевания для назначения рационального лечения. Факторы, от которых зависит прогноз ОМЛ у детей, разделяют на клинические и лабораторные. К клиническим можно отнести возраст, пол, анамнез, размеры паренхиматозных органов, выраженность геморрагического синдрома, инициальное поражение ЦНС, время наступления ремиссии, количество курсов химиотерапии. Среди лабораторных прогностических факторов выделяют чувствительность бластных клеток к химиопрепаратам in vitro, количество лейкоцитов в анализе периферической крови, FAB-вариант ОМЛ, уровень фибриногена, уровень лактатдегидрогеназы, наличие палочек Ауэра в бластах.
Прогноз при ОМЛ зависит от FAB-морфологического варианта, данных генетического исследования и иммунофенотипа бластных клеток. Так, наиболее благоприятную группу составляют больные с морфологическими вариантами М1, М2 и t(8;21), t(9;11), М3 и t(15;17) или М4 и inv(16). В неблагоприятную для прогноза группу входят больные с вариантами М4 без inv(16), М5, М6 и М7, а также пациенты, при исследовании кариотипа опухолевых клеток которых были выявлены следующие хромосомные аномалии: t(9;22), t(6;11), t(10;11), del5q-, del7q-, моносомии -5, -7. Кроме того, нашими исследованиями удалось доказать, что на прогноз ОМЛ неблагоприятно влияет экспрессия эритроитных и В-линейных антигенов на поверхности бластов.
Происхождение[править | править код]
Миелобласты происходят в конечном счёте от примитивных стволовых клеток ретикулума, так называемых гемангиобластов, находящихся между клетками стромы костного мозга. В процессе созревания и дифференцировки от гемангиобласта до миелобласта клетка проходит ещё несколько стадий: гемоцитобласт (плюрипотентная стволовая кроветворная клетка), CFU-GEMM (промиелобласт), CFU-GM (миеломонобласт). На каждой из стадий дифференцировки выбор возможных путей развития для клетки сужается. Так, на стадии гемангиобласта у клетки есть возможность стать либо кроветворной клеткой, либо клеткой эндотелия сосудов. На стадии гемоцитобласта этого выбора уже нет — клетка рекрутирована в кроветворный росток. Но сохраняется возможность дифференцировки по любому из путей дифференцировки кроветворных клеток — миелоидному или лимфоидному. На стадии CFU-GEMM возможность развития по лимфоидному пути уже закрыта, так как клетка уже избрала миелоидный путь дифференцировки, однако она всё ещё может выбрать разные пути дальнейшего развития — эритроидный, мегакариоцитарный или миеломоноцитарный. На стадии CFU-GM клетке остаётся возможность выбора уже только между моноцитарным и гранулоцитарным путём развития (эритроцитарный и тромбоцитарный пути развития для неё уже закрыты). И наконец, на стадии миелобласта клетка уже полностью унипотентная, избравшая гранулоцитарный путь развития. Процессы гранулопоэза и рекрутирования клеток-предшественников в ту или иную клеточную линию регулируются гуморальными агентами — цитокинами и хемокинами, такими, как колониестимулирующие факторы, интерлейкин 3.
Хронический миелолейкоз
Хроническую форму миелолейкоза характеризует ускоренное и нерегулируемое размножение миелоидных клеток костного мозга, которые быстро накапливаются в кровеносном русле. Как и ОМЛ, хронический миелоидный лейкоз имеет несколько видов, которые определяют дальнейшую тактику лечения:
- наличие филадельийской хромосомы;
- ювенильная форма;
- нейтрофильная или эозинофильная форма;
- первичный миелофиброз.
Причины и отличия от острого

Среди причин развития хронического миелолейкоза выделяют те же факторы, что и при ОМЛ:
- радиоактивное или ионизирующее излучение;
- использование препаратов из ряда цитостатиков;
- наследственная предрасположенность к заболеванию.
Выделяют несколько отличительных черт, которые позволяют дифференцировать хроническую форму заболевания от острого миелолейкоза. Обычно клетки костного мозга при ХМЛ успевают созреть, но большинство из них не в состоянии корректно выполнять свои главные функции. В крови наблюдается значительное уменьшение количества эритроцитов, много белых кровяных телец, однако выполнять свое предназначение они неспособны.
По этой причине развивается недостаточность органов или систем, так как ткани не получают достаточное количество кислорода. Кроме того, организм не может самостоятельно и эффективно бороться с вирусными и бактериальными инфекциями, так как костный мозг не регулирует достаточный синтез антител.
Клиника
На долю ХМЛ от числа всех лейкозов приходится всего до 14% зарегистрированных случаев. Чаще всего болезнь появляется у мужчин в преклонном возрасте, но может быть выявлена и у детей. Клиника хронического миелолейкоза выражена значительно менее, чем острого. Заболевание протекает медленно – пик развития наступает примерно через 2-3 года после начала.
Основные ХМЛ симптомы:
- общая слабость, потеря работоспособности;
- повышение температуры тела;
- увеличение селезенки и печени.
Кроме того, иногда ремиссия отмечается сразу после непродолжительного лечения. При этом подобные периоды облегчения достаточно быстро сменяются рецидивами без назначения определенного лечения.
Очень важно правильно поставить дифференциальный диагноз, чтобы лечение было адекватным заболеванию. Если его не удается взять под контроль, оно достаточно быстро переходит на терминальную стадию. Конечная стадия ХМЛ в большинстве случаев заканчивается смертью пациента, несмотря на проводимую терапию
Конечная стадия ХМЛ в большинстве случаев заканчивается смертью пациента, несмотря на проводимую терапию.
Лечение хронического миелоидного лейкоза
Главное направление терапии – использование высокоэффективных лекарственных препаратов цитостатического ряда, назначение которых зависит от стадии заболевания. Средства оказывают непосредственное действие на раковые клетки, останавливая их деление и рост опухоли.
Кроме цитостатиков, назначается лучевая терапия, пересадка здорового костного мозга, многочисленные переливания крови с функционирующими кровяными тельцами. Такие методы лечения используют при недостаточной эффективности консервативной медикаментозной терапии или для поддержки действия препаратов.
Прогноз для жизни
Обычно хроническая форма миелолейкоза не поддается лечению, и большинство пациентов погибает на терминальной стадии болезни. Продолжительность жизни людей, у которых был диагностирован хронический миелоидный лейкоз, составляет 1,5-2 года. При терминальной стадии пациенты погибают через 3-4 месяца после бластного криза.
Диета
Диета при лейкозе (рак крови)
- Эффективность: нет данных
- Сроки: до выздоровления/пожизненно
- Стоимость продуктов: 3000-4600 руб. в неделю
В период лечения важно придерживаться рекомендаций по поводу правильного питания. Правильный рацион с достаточным содержанием важных для организма веществ поспособствует эффективности лечения болезни
В ходе лечения миелолейкоза очень важно не допускать дефицита железа, кобальта, меди, марганца, никеля, а также витамина С. Все эти компоненты важны для восстановления кровяных телец, а также для поддержания оптимального общего состояния больного. В рацион следует ввести такие продукты:
- белковую пищу – морскую рыбу и морепродукты, мясо кролика и птицы, яичные желтки, субпродукты, молочные продукты;
- овощи – зелень, перец, капусту, бобовые, морковь, тыкву, кукурузу, кабачки;
- фрукты – цитрусовые, грушу, ягоды, яблоки, сливу, персики, абрикос, облепиху;
- крупы;
- хлеб с отрубями;
- мед.
Рекомендуется исключить из рациона:
- баранину и говядину, которые содержат тугоплавкий жир;
- кофе, чай и другие продукты, содержащие кофеин;
- продукты с уксусом – консервацию и др.;
- алкоголь;
- острые специи.
Рекомендуется снизить количество потребляемых жиров.
Расположение в организме[править | править код]
Миелобласты, как и другие кроветворные клетки, находятся в экстраваскулярных (внесосудистых) пространствах костного мозга. Гемопоэз происходит в этих экстраваскулярных (внесосудистых) полостях или пространствах между синусами костного мозга. Стенки синусов костного мозга выстланы двумя типами клеток — эндотелиальными клетками и адвентициальными ретикулярными клетками. Гемопоэтические стволовые клетки расположены в виде равномерных полос, шнуров или клиньев между этими сосудистыми синусами. При этом миелобласты и другие гранулоцитарные клетки-предшественники расположены в основном в субкортикальных («подкорковых», наиболее близких к корковому слою, то есть к поверхности синуса) этих гемопоэтических «шнуров» или клиньев.
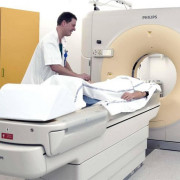
Острый миелобластный лейкоз – что это такое?
Под ОМЛ подразумевается группа онкопатологий, при которых злокачественный процесс захватывает миелоидный росток клеток крови в костном мозге. Поврежденная часть клетки подавляет собой здоровые элементы, после чего клетка становится неполноценной и неспособной вырасти до зрелого состояния.
Пораженные клетки быстро делятся, образуя себе подобные, выходят из мест локализации, попадают в кровеносное русло и с током крови разносятся по организму больного. Таким образом прогрессирует это заболевание.
Острыми эта группа лейкозов называется по той причине, что мутации подвергаются именно незрелые клетки крови, а состояние пациента при отсутствии грамотно назначенного лечения ухудшается с высокой скоростью.
В группу ОМЛ входят:
- миеломонабластный лейкоз;
- миеломоноцитарная лейкемия;
- монобластная форма моноцитарного типа;
- мегакариобластный рак крови;
- эритробластный лейкоз.
Они отличаются между собой объектом мутации и путем развития. Определить, какой именно формой ОМЛ болен пациент, можно только после тщательного обследования на основании полученных результатов.
Как продлить срок жизни
Срок жизни при миелоцитарном лейкозе может быть увеличен при соблюдении ряда рекомендаций.
Лечение необходимо начинать сразу после обнаружения онкологического заболевания. Рекомендуется регулярно проходить осмотры у врача: это поможет избежать развития запущенных форм патологии.
Потребуется коррекция питания. Из рациона необходимо исключить все продукты, содержащие канцерогенные добавки. Рекомендуется употреблять в пищу натуральные продукты без усилителей вкуса, красителей, консервантов.
От вредных привычек рекомендуется отказаться. Курение и употребление алкогольных напитков может негативно повлиять на состояние больного. Отказ от вредных привычек рекомендован и при достижении стойкой ремиссии: это поможет избежать рецидива.
Необходимо соблюдать все рекомендации лечащего врача. Отказываться от терапии в пользу народных методик не стоит: это может стать причиной гибели пациента
Прием лекарств важно проводить курсом. Пропуски, самовольная преждевременная отмена препаратов недопустимы. Если имеется наследственная предрасположенность, важно регулярно проходить обследования
Это поможет избежать развитие болезни
Если имеется наследственная предрасположенность, важно регулярно проходить обследования. Это поможет избежать развитие болезни. Важен настрой пациента
Активные, жизнерадостные люди живут дольше, чем уверенные в скорой гибели больные
Важен настрой пациента. Активные, жизнерадостные люди живут дольше, чем уверенные в скорой гибели больные.
Необходимо укреплять иммунную систему. Поскольку при онкологических заболеваниях организм ослаблен, вероятность заражения инфекционными патологиями возрастает. Кроме того, болезни тяжело протекают, вызывают общее ухудшение состояния человека
Важно употреблять достаточное количество витаминов. Может потребоваться прием специального комплекса, подбирать который следует вместе с доктором
Диагностика ОМЛ
Так как все рассмотренные симптомы ОМЛ не являются достоверными признаками болезни, существует четко регламентированная диагностика заболевания:
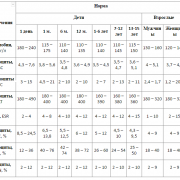
Общеклинический анализ крови. Первый и немаловажный метод ранней диагностики
Даже при этом общедоступном анализе можно обнаружить отклонения, а своевременное обнаружение бесспорно важно для успешного лечения. При микроскопическом обследовании обнаруживается, что количество эритроцитов и тромбоцитов неуклонно падает, а уровень злокачественных видов лейкоцитов (бластных клеток), растет
Отсутствие «здоровых» лейкоцитов приводит к состоянию так называемого бластного криза. Также его называют лейкимический провал.
Биохимическое исследование крови. Этот анализ не является основным показателем для диагностики заболевания, но повышение витамина В12, некоторых ферментов, мочевой кислоты, могут стать основанием для более тщательной диагностики.
Пункция костного мозга. Также называют биопсией костного мозга. Данный анализ считается самым точным при диагностике ОМЛ. Из грудины или из крыла подвздошной кости берутся образцы костного мозга. Данный диагноз подтверждается при обнаружении незрелых лейкоцитов превышающих норму.
Другими методами являются: ЭКГ, общий анализ мочи, рентген легких, УЗИ внутренних органов. Как было указано, при лейкозе нарушается работа внутренних органов, следовательно, данные виды обследования могут подтверждать диагноз при каких-либо отклонениях.
Генетическое исследование. При данной диагностике наблюдаются хромосомные нарушения. Их изучение дает возможность определить метод лечения и сделать прогнозы. Существуют так называемые морфологические варианты, которые дают благоприятный прогноз. Таковыми являются М1, М2, М3, М4. Считается, что другие формы часто вызывают рецидивы.
Выживаемость
При диагностировании монобластного лейкоза для его лечения необходимо обратиться к онкологу и гематологу.
По теме
Онкогематология
Зуд при лимфоме
- Ольга Владимировна Хазова
- 16 октября 2020 г.
Для получения прогностических данных важно принимать во внимание несколько основополагающих показателей:
- возрастная категория, к которой относится больной;
- стадия развития онкологического процесса;
- степень вовлеченности в заболевание других анатомических структур;
- время, когда именно была обнаружен болезнь;
- эффективность проводимого лечения.
На продолжительность жизни пациента будет влиять уровень поражения костного мозга и переносимость терапевтических процедур.
Если заболевание находится на острой стадии, то средняя выживаемость составляет примерно от одного до трех месяцев.
Если больной хорошо переносит лечение, и его состояние не ухудшается, то данные показатели могут составлять до трех лет жизни.