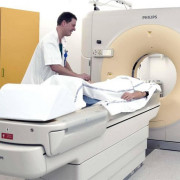
Как лечится респираторный дистресс-синдром новорожденных
Содержание:
Клиника и диагностика
Пренатальный диагноз основан на оценке
зрелости легких плода по фосфолипидному
составу околоплодной жидкости и оценке
уровня сурфактантного протеина А.
У новорожденного первым признаком
развивающегося СДР является одышка,
которая обычно появляется через 1-4 часа
после рождения. Одышка при СДР возникает
на фоне розовых кожных покровов, так
как имеется большое сродство фетального
гемоглобина к кислороду.
Экспираторные шумы обусловлены тем,
что на начальных этапах СДР в качестве
компенсаторного механизма развивается
спазм голосовой щели на выдохе,
способствующего увеличению остаточной
емкости легких и препятствующего
спадению альвеол.
Западение грудной клетки на выдохе –
третий по времени появления признак
СДР. Позднее возникает напряжение
крыльев носа, приступы апноэ, цианоз,
раздувание щек, ригидный сердечный
ритм, парадоксальное дыхание, пена у
рта, отек кистей и стоп, плоская грудная
клетка.
Аускультативно в первые часы жизни над
легкими выслушивается резко ослабленное
дыхание, далее на фоне ИВЛ – нормальные
дыхательные шумы, позднее – высокие
сухие хрипы на вдохе и выдохе, крепитирующие
и мелкопузырчатые хрипы.
Общие симптомы: температурная
нестабильность, вялость, бледность
движений, гипорефлексия, атрериальная
и мышечная гипотония, олигурия, срыгивания,
вздутие живота, периферические отеки,
большие потери первоначальной массы
тела. Нижние конечности часто находятся
в «позе лягушки». При прогрессировании
развиваются признаки шока и ДВС-синдрома.
Тяжесть дыхательных расстройств у
новорожденных оценивается по шкале
Сильвермана.
Шкала Сильвермана
|
Стадия 0 |
Стадия I |
Стадия II |
|
Верхняя часть грудной клетки и передняя
Отсутствие втяжения межреберий на
Отсутствие втяжения мечевидного
Отсутствие движения подбородка при Отсутствие шумов на выдохе. |
Отсутствие синхронности или минимальное Легкое втяжение межреберий на вдохе.
Небольшое втяжение мечевидного
Опускание подбородка на вдохе, рот
Экспираторные шумы слышны при |
Заметное западение верхней части Заметное втяжение межреберий на вдохе.
Заметное западение мечевидного
Опускание подбородка на вдохе, рот
Экспираторные шумы слышны при поднесении |
Примечание: каждый симптом в графе
«Стадия I» оценивается в 1 балл, в графе
«Стадия II» — в 2 балла.
Клиническая форма развития синдрома
дыхательных расстройств расценивается
как:
— крайне тяжелая при оценке по шкале
Сильвермана в 10 баллов
— тяжелая – 6-9 баллов
— средней тяжести – 5 баллов
— начинающийся СДР – менее 5 баллов
Осложнения у новорожденных с СДР
|
Системные осложнения |
Местные осложнения |
|
— незаращение артериального протока — септический шок — ДВС-синдром — внутрижелудочковые кровоизлияния — гипогликемия — транзиторная гипераммониемия — ядерная желтуха |
— синдром «утечки воздуха» — кровоизлияния в легкие — пневмонии — бронхолегочная дисплазия — связанные с интубацией: — поражения гортани — поражения трахеи |
Помимо клинических данных, для диагностики
СДР обязательно используют рентгенологическое
исследование грудой клетки. Характерна
триада симптомов:
— диффузные очаги пониженной прозрачности
— воздушная бронхограмма
— пониженная пневматизация легочных
полей в нижних отделах легких и на
верхушках
Мониторное наблюдение проводится за
всеми новорожденными с синдромом
дыхательных расстройств и включает:
— контроль частоты сердечных сокращений
и дыханий
— чрескожную оксигемоглобинометрию
— термометрия кожи живота каждые 3-4 часа,
определение артериального давления,
диуреза, КОС, уровня гликемии и концентрации
О2 во вдыхаемом воздухе
— Rg-графию грудной клетки (ежедневно в
острой фазе)
— проведение клинического анализа крови,
посева крови и содержимого трахеи,
определение гематокрита
— определение в сыворотке крови уровня
мочевины, калия, натрия, кальция и магния,
общего белка и альбуминов, осмолярность
крови.
Причины
Среди причин развития ОРДС у взрослых выделяют легочные (прямые) и внелегочные (непрямые) повреждающие факторы:
- К легочным факторам относятся: ушибы/травмы легких, инфекционно-воспалительные заболевания легких, пневмоторакс, аспирация жидкости, радиационный пневмонит, легочное кровотечение, тромбоэмболия легочной артерии, отравление токсическими газами, трансплантация легкого.
- К внелегочным факторам относятся: массивная гемотрансфузия, сепсис, ожоги, тяжелые неторакальные травмы, шок, передозировка лекарств/наркотических средств, обширные оперативные вмешательства, уремия, ДВС-синдром, онкозаболевания, панкреонекроз, системные патологии, сильное переохлаждение/перегревание организма, электротравма, утопление.
К основным причинам развития РДС у новорожденных относятся:
- нарушение процесса выработки/экскреции сурфактанта альвеолоцитами, обусловленное структурной/функциональной незрелостью тканей легких;
- врожденный (генетически обусловленный) дефект структуры сурфактанта.
Предрасполагающими факторами развития РДС у ребенка являются:
- дистресс плода, обусловленный различными негативными внутриутробными факторами (внутриутробная гипоксия, гемолитическая болезнь плода, асфиксия в родах, преждевременная отслойка плаценты и др.);
- пневмопатия у новорожденных (морфофункциональная незрелость тканей легких, аспирация околоплодных вод, ателектазы легких, отечно-геморрагический синдром и др.);
- преждевременные роды/кесарево сечение при отсутствии родовой деятельности;
- сахарный диабет 1-го типа у матери;
- недоношенность;
- асфиксия новорожденного;
- охлаждение ребенка, гиповолемия.
Патогенез
Синдром начинается с повышения проницаемости легочных капилляров для белков, далее снижается градиент онкотического давления между плазмой и интерстициальной тканью, жидкость начинает поступать из плазмы крови в интерстициальную ткань. В этих условиях даже самое незначительное увеличение гидростатического давления в легочных капиллярах (вследствие инфузионной терапии и нарушения функции сердца) приводит к резкому усилению альвеолярного и интерстициального отек легких . В связи со значительной ролью повышения гидростатического давления изменения более выражены в нижележащих отделах легких. Происходит, с одной стороны, накопление в ткани легких жидкости, с другой — снижение объема альвеол.
Из-за повреждения альвеолоцитов II типа снижается продукция сурфактанта, изменяется его состав. Как следствие, транспульмональное давление, поддерживающее альвеолы в открытом состоянии, становится меньше их эластической тяги, развиваются ателектазы . Падает податливость легких.
В непораженных участках легких вентиляция и газообмен происходят относительно нормально. Поскольку вентиляторная и газообменная функции ложатся целиком на них, можно образно сказать, что функцию внешнего дыхания во взрослом организме обеспечивает пара детских легких.
Из-за снижения податливости легких дыхательные мускулатура на вдохе развивает большие усилие, в результате чего резко возрастает работа дыхания и развивается усталость дыхательных мышц. Гипоксемия и возбуждение механорецепторов обуславливают тахипноэ. Все это приводит к дальнейшему снижению дыхательного объема и ухудшению газообмена.
Из-за сужения бронхов, вызванного отеком и бронхоспазмом, уменьшается числа бронхов, по которым движется воздух, повышается сопротивление дыхательных путей. Легочное сосудистое сопротивление и давление в легочной артерии увеличиваются: сначала под влиянием нейрогуморальных факторов, позже — вследствие обструкции, окклюзии и перестройки легочных сосудов.
Газообмен харастеризуется снижением VA/Q , значительным внутрилегочным сбросом крови справа налево и увеличением мертвого пространства. Внутрилегочный сброс крови обусловлен ателектазами и ослаблением гипоксической вазоконстрикции, а объем мертвого пространства увеличивается из-за обструкции и окклюзии легочных капилляров.
Проявления патологии
Заболевание проявляется сразу после рождения ребенка или в течение первых суток его жизни.
- синюшность кожи;
- раздувающиеся ноздри при дыхании, трепетание крыльев носа;
- западение податливых участков грудной клетки (мечевидного отростка и области под ним, межреберных промежутков, зон над ключицами) на вдохе;
- быстрое поверхностное дыхание;
- уменьшение количества выделяемой мочи;
- «стоны» при дыхании, возникающие вследствие спазма голосовых связок, или «экспираторное хрюканье».
Дополнительно врач фиксирует такие признаки, как низкий тонус мышц, снижение артериального давления, отсутствие стула, изменение температуры тела, отечность лица и конечностей.
Профилактика
Специфическая профилактика ОРДС отсутствует. Чтобы предотвратить развитие патологии, необходимо остерегаться воздействия стрессовых повреждающих факторов: своевременно лечить инфекционные заболевания легких, избегать травм грудной клетки, не вдыхать токсические вещества. Врачам следует тщательно контролировать процесс переливания крови.
- Для этого беременным женщинам назначают «Дексаметазон», «Бетаметазон», которые способствуют созреванию сурфактанта в легких. Польза правильного профилактического применения лекарственных препаратов для новорожденного должна превосходить потенциальный риск и выражаться в снижении перинатальной заболеваемости и смертности.
- Для лечения гипертензии беременным назначают «Эуфиллин».
- Легкие быстрее созревают у плода под влиянием «Фолликулина», «Метионина», «Эссенциале», «Лазолвана» и «Бромгексина».
Профилактику дистресс-синдрома не проводят женщинам на сроке более 34 недель.
Своевременная диагностика ОРДС и адекватная терапия позволяют вылечить даже новорожденных. В противном случае дистресс-синдром приводит к смерти больных. При развитии полиорганной недостаточности частота летальных исходов возрастает во много раз. Смертность больных зависит от легочной дисфункции. После перенесенного заболевания легкие могут восстановить почти нормальную функцию.
Выбор токолитика
На сегодняшний день наиболее распространенным и наиболее изученным в плане материнских и перинатальных эффектов являются селективные β2-адреномиметики, представителями которых в нашей стране являются гексопреналина сульфат и фенотерол.
Противопоказания для использования β-адреномиметиков:
сердечно-сосудистые заболевания матери (стеноз устья аорты, миокардит, тахиаритмии, врожденные и приобретенные пороки сердца, нарушения сердечного ритма);
закрытоугольная форма глаукомы;
инсулинзависимый сахарный диабет;
дистресс плода, не связанный с гипертонусом матки.
со стороны матери: тошнота, рвота, головные боли, гипокалиемия, повышение уровня глюкозы крови, нервозность/беспокойство, тремор, тахикардия, одышка, боли в груди, отек легких;
со стороны плода: тахикардия, гипербилирубинемия, гипокальциемия.
N.B. Частота побочных эффектов зависит от дозы β-адреномиметиков. При появлении тахикардии, гипотонии скорость введения препарата должна быть снижена, при появлении загрудинных болей введение препарата необходимо прекратить.
Рекомендуемые схемы : Гексопреналина сульфат
токолиз следует начинать с болюсного введения 10 мкг (1 ампула по 2 мл) препарата, разведенного в 10 мл изотонического раствора, в течение 5-10 минут (острый токолиз) с последующей инфузией со скоростью 0,3 мкг/мин (массивный токолиз). Расчет дозы:.
Причины
Название болезни указывает на патологию у взрослых потому, что что она отличается от дистресс-синдрома новорожденных одним принципиальным моментом. Заболевание у появившихся на свет детей обусловлено врожденной нехваткой сурфактанта – вещества, которое, покрывая изнутри альвеолы, держит их в тонусе, не давая спадаться, тем самым поддерживает воздушность легких. У взрослых же нехватка сурфактанта развивается вторично. Таким образом причинно-следственные связи этого заболевания у детей и взрослых – противоположные.
Чаще всего дистресс-синдром взрослых наступает при таких заболеваниях и состояниях дыхательной системы, как:
- воспаление легких самого разного происхождения – чаще всего это бактериальные, вирусные и грибковые пневмонии;
- состояние длительного сдавливания грудной клетки (например, случившегося из-за обвалов домов при землетрясении);
- выраженные травмы грудной клетки, при которых костные отломки ранят легочную ткань;
- попадание (аспирация) в легкие рвотных масс или воды (в случае утопления);
- эмболия (закупорка) ветвей легочной артерии тромбом, пузырьками воздуха, жировыми частицами, конгломератами паразитов и их яиц, скоплениями опухолевых клеток, а у новорожденных – амниотической жидкостью (жидкой средой, окружающей плод в время внутриутробного развития);
- вдыхание ядовитых веществ – в первую очередь, деструктивным действием на легочную ткань обладают закись азота, хлор, аммиак, фосген. Длительное вдыхание чистого кислорода может иметь такой же эффект;
- длительное пребывание в условиях высокогорья с разжиженным воздухом.
Дистресс-синдром также могут вызвать заболевания и состояния, которые напрямую не затрагивают легкие – это:
- анафилактический (аллергический) шок;
- септический шок, возникающий по причине тотального отравления организма, при котором яды могут попасть в него разными путями – через органы дыхания, пищеварительный тракт и так далее;
- ДВС-синдром, или синдром диссеминированного (распространенного) внутрисосудистого свертывания крови – состояние, при котором во многих участках кровеносного русла образуются мелкие тромбы;
- чрезмерная нагрузка венозной системы жидкостью (отмечается при интенсивном внутривенном капельном введении инфузионных растворов);
- интенсивное переливание крови, при котором в сосудах легких развивается множественное тромбообразование;
- тяжелые нарушения химически процессов в организме (например, уремия, при которой нарушается выведение с мочой токсических веществ, и они попадают в ток крови);
- острый панкреонекроз (омертвение поджелудочной железы) с выделением большого количества ферментов, из-за чего возникает разрушение тканей – в частности, легочной ткани;
- аутоиммунные заболевания – патологии, при которых организм начинает вырабатывать антитела против собственных же тканей. В первую очередь это синдром Гудпасчера (образование антител к клеткам почек и легких) и системная красная волчанка (поражение соединительной ткани и сосудов во многих органах – в данном случае в легких);
- длительное подключение к аппарату искусственного кровообращения.
Синдром дыхательных расстройств у новорожденных
Подробности 14 ноября 2016 Синдром дыхательных расстройств (СДР), по данным ВОЗ, занимает одно из ведущих мест в структуре перинатальной смертности. Летальность детей с СДР, по данным различных авторов, составляет от 35 до 75%. Чаще встречается у недоношенных детей, реже — у доношенных. К. А.
Сотникова указывает, что термин “синдром дыхательных расстройств” является условным.
По ее определению, “под синдромом дыхательных расстройств подразумевают особое клиническое состояние новорожденного, которое характеризуется ранним возникновением (в первые 2 сут жизни) и зачастую бурным нарастанием на фоне значительного угнетения жизненно важных функций организма симптомов дыхательной недостаточности”.
Одной из основных причин СДР являются пневмопатии (гиалиновые мембраны, ателектазы, обширные кровоизлияния в легких, отечно-геморрагический синдром, врожденные пороки развития легких, спонтанный пневмоторакс) и внутриутробные пневмонии.
В патогенезе, независимо от причины, вызвавшей СДР, основное значение имеют дефицит сурфактанта и обтурационный синдром, гипоксия, метаболический ацидоз, нарушениеобмена веществ, приводящие кизменению гомеостаза и нарушению функций центральной и вегетативной нервной системы, эндокринной и сердечно-сосудистой систем, нарушению соотношения между вентиляцией и кровотоком, угнетению иммунитета. Большое значение имеют нарушение соотношения между вентиляцией и кровотоком в легких, повышение проницаемости сосудов. Дефициту сурфактанта в настоящее время придают ведущее значение в патогенезе. Считают, что полностью система сурфактанта созревает к 35–36-й неделе внутриутробного развития. У ребенка, родившегося до этого срока, имеющиеся запасы сурфактанта обеспечивают начало дыхания, его недостаток приводит к спадению альвеол на выдохе, резкому возрастанию работы дыхательных мышц. Вследствие спадения альвеол непрерывного газообмена в легких не происходит, что приводит к развитию гипоксемии, гиперкапнии.
Диагноз СДР традиционно ставится на основании данных анамнеза, клинических и рентгенологических симптомов. Рентгенологически определяется характерная для СДР триада признаков, появляющаяся уже в первые часы заболевания:
- диффузное снижение прозрачности легочных полей
- ретикулогранулярная сетчатость
- наличие полосок просветления в области корня легкого (воздушная бронхограмма)
В тяжелых случаях возможно тотальное затемнение легочных полей, границы сердца могут не дифференцироваться.
В последнее время в арсенале медиков появились методы, определяющие степень зрелости как самой легочной ткани, так и системы сурфактанта.
В качестве самого распространенного и информативного теста используется определение отношения лецитина к сфингомиелину в околоплодных водах, трахеальной жидкости или аспирате содержимого желудка при рождении.
Используется также «пенный» тест: при добавлении этанола в жидкость, содержащую сурфактант, и встряхивании образуется пена.
Эти же методы могут использоваться и при пренатальной дианостике, но вопрос об амниоцентезе должен решаться индивидуально и при сроке беременности не менее 32 недель, так как в более ранние сроки гестации незрелость легких не вызывает сомнений, а ведение беременности предполагает минимум инвазивных исследований.
Этиологическим методом лечения является введение экзогенных сурфактантов. Применение их возможно как с профилактической, так и с терапевтической целью.
Препараты сурфактанта относятся к четырем категориям:
- естественные препараты, полученные из амниотической жидкости человека (при разрешении доношенной беременности путем кесарева сечения)
- естественные препараты, полученные из измельченных легких поросят и телят
- полусинтетические смеси измельченных легких теленка с дипальмитоилфосфатидилхолином (ДПФХ)
- полностью синтетические сурфактантные препараты.
При применении естественных сурфактантов быстрее наступает клинический эффект, но конечные результаты лечения не отличаются от таковых при назначении искусственных сурфактантов.
Предполагается, что сурфактант, выделенный из легких телят и поросят, может вызвать иммунологическую реакцию на чужеродный белок, но убедительных данных получено не было.
Наиболее естественный для ребенка сурфактант из амниотической жидкости не может широко использоваться, так как для лечения одного ребенка требуется использование амниотической жидкости от 10 операций кесарева сечения.
Краткая информация
1.1 Определение
Преждевременные роды (ПР):
- беременность 22 — 36 недель + 6 дней (154 — 259 дней), отсчёт с 1-го дня последней нормальной менструации при регулярном цикле
- масса тела плода 500-2500 г.
1.2 Этиология и патогенез
Преждевременные роды — «большой акушерский синдром»
Причины развития:
- материнские
- отцовские
- фетальные
- средовые факторы.
Основные группы причин ПР по Lockwood C. с соавт. (2005 г.):
- инфекционно-воспалительные – 40%
- активация материнско-плодовой гипоталамо-гипофизарно-надпочечниковой системы — 30%
- кровотечения — 20%
- перерастяжение матки -10%.
Очень часто сочетание факторов не позволяет определить ведущую причину ПР.
Патогенетические состояния:
- увеличение количества и активности окситоциновых рецепторов
- коагулопатии с последующим тромбозом
- инфекции, приводящие к повышению уровня провоспалительных цитокинов
- иммунологические и генетические особенности взаимоотношения матери и плода
- гормональные нарушения
- анатомические изменения половых органов врожденные или вследствие оперативных вмешательств.
1.3 Эпидемиология
Частота в развитых странах 5-7%, неонатальная смертность – до 28%.
Ежегодно в мире рождается 15 миллионов недоношенных детей.
Тяжесть осложнений, связанных с недоношенностью, пропорциональна гестационному сроку ПР.
1.4 Кодирование по МКБ-10
O60 — Преждевременные роды
O42 — Преждевременный разрыв плодных оболочек
О42.0 — Преждевременный разрыв плодных оболочек, начало родов в последующие 24 часа
O42.1 — Преждевременный разрыв плодных оболочек, начало родов после 24- часового безводного периода
O42.2 — Преждевременный разрыв плодных оболочек, задержка родов, связанная с проводимой терапией
1.5.1 Классификация ПР в соответствии со сроком гестации:
До 28 недель (27 недель 6 дней) — очень ранние ПР:
- 5% всех преждевременных родов;
- новорожденные глубоко недоношенные;
- экстремально низкая масса тела (до 1000 г);
- выраженная незрелость легких;
- прогноз для новорожденного крайне неблагоприятный;
- заболеваемость и смертности новорожденных крайне высокие.
28-30 недель 6 дней — ранние ПР:
- 15% всех преждевременных родов;
- тяжелая недоношенность;
- очень низкая масса тела (до 1500 г);
- легкие незрелые;
- исход родов для плода и постнатальный прогноз более благоприятны.
31-33 недели 6 дней — преждевременные роды:
- 20% всех преждевременных родов;
- недоношенность средней степени.
34-36 недель 6 дней — поздние преждевременные роды:
- 70% всех преждевременных родов;
- легкие плода практически зрелые;
- инфекционная заболеваемость новорожденных значительно ниже;
- пролонгирование беременности не оказывает существенного влияния на смертность новорожденных.
Респираторный дистресс-синдром новорожденных
Респираторный дистресс-синдром новорожденных (синдром дыхательных расстройств) – неинфекционные патологические процессы (первичные ателектазы, болезнь гиалиновых мембран, отечно-геморрагический синдром), формирующиеся в пренатальном и раннем неонатальном периодах развития ребенка и проявляющиеся нарушением дыхания. Частота развития респираторного дистресса зависят от степени недонашивания и составляет в среднем 60 % у детей, родившихся при сроке беременности менее 28 недель, 15-20 % – при сроке 32-36 недель и 5 % – при сроке 37 недель и более. При рациональном выхаживании таких детей летальность приближается к 10 %.
Большинство детей рождаются в состоянии асфиксии и врожденной гипоксии, но расстройства дыхания могут появиться не сразу, а спустя несколько часов после рождения.
Типичными являются резко выраженные признаки дыхательной недостаточности: одышка с частотой дыханий 60 и более в 1 мин (нередко с апериодическим дыханием), цианоз (периоральный, акроцианоз, генерализованный), бледность кожных покровов, участие в акте дыхания вспомогательной мускулатуры (напряжение крыльев носа, втяжение уступчивых мест грудной клетки – межреберных промежутков, мечевидного отростка грудины, втягивание надключичных ямок), ригидность грудной клетки, иногда пена у рта, затрудненный “ворчащий” вдох (спазм ой щели), раздувание щек. Отмечается снижение двигательной активности, гипорефлексия, мышечная гипотония. Для раннего выявления и оценки тяжести дыхательных расстройств у новорожденных используют шкалу Сильвермана. Оценка производится в динамике каждые 6 ч на протяжении 2-3 дней.
По мере прогрессирования болезни дыхательные расстройства и симптомы угнетения нервной системы нарастают, усиливается цианоз, появляются апноэ, “хрюкающий” выдох и парадоксальное дыхание (при выдохе передненижние отделы грудной клетки втягиваются, а живот выпячивается), рассеянная крепитация.
Часто появляются местные и генерализованные отеки; пенистые, иногда кровянистые выделения изо рта.
Поражается сердечно-сосудистая система, наблюдаются тахикардия, глухие тоны сердца, сохраняются плодовые коммуникации с праволевым шунтом, нарастают признаки легочной гипертензии, развивается кардио- и гепатомегалия.
Описание
Развивается в основном у недоношенных детей от матерей с отягощенным акушерским анамнезом (сердечно-сосудистые заболевания, сахарный диабет, нефропатии, патология плаценты, маточные кровотечения). Имеет значение внутриутробная гипоксия, асфиксия и гиперкапния в родах при наличии незрелости ткани легкого.
Под действием гипоксии и гиперкапнии наступает нарушение легочного кровообращения, происходит пропитывание межальвеолярных перегородок серозной жидкостью с выходом в просвет альвеол составных частей плазмы, в частности фибрина. Образование гиалиновых мембран возможно и в результате снижения фибринолитической активности крови.
Отмечается также отсутствие или резкое снижение активности антиателектатического фактора (сурфактанта), что способствует возникновению ателектазов. Определенное значение имеет дефицит плазминогена, альфа2-макроглобулина и развитие локального или диссеминированного внутрисосудистого свертывания крови.
Отмечаются недоразвитие эластической ткани легкого, незрелость альвеол, аспирация околоплодной жидкости и слизи, особенно у глубоконедоношенных детей.
Симптомы
В клинической картине респираторного дистресс-синдрома взрослых медики выделяют четыре периода. Первый является скрытым (когда происходит влияние фактора-причины). Длится период сутки после контакта организма с причинным фактором. Происходит патофизиологические и патогенетические изменения. Но никакие симптомы не проявляются, изменений на рентгенограмме также нет. Но в этом периоде у больного можно обнаружить тахипноэ, когда он делает более 20 дыханий за минуту.
Второй период называется периодом начальных изменений. Он фиксируется в 1-2 сутки от начала действия этиологического фактора. Начинают выявляться симптомы, прежде всего, это тахикардия и выраженая одышка. Аускультативные методы определяют жесткое везикулярное дыхание и рассеянные сухие хрипы. Рентген обнаруживают усиление сосудистого рисунка, особенно в периферических отделах. Такие изменения говорят, что начинается интерстициальный отек легких. Исследование газового состава крови не показывает отклонений, или может быть выявлено незначительное снижение РаО2.
Третий период называется развернутым или периодом выраженных клинических проявлений. Симптомы выражены ярко, говорят об острой дыхательной недостаточности. У человека наблюдают выраженную одышку. В акте дыхания принимает участие вспомогательная мускулатура. Наблюдается раздуванием крыльев носа, втягивание межреберных промежутков. Также хорошо выражен диффузный цианоз. При аускультации сердца обнаруживают глухость сердечных тонов и тахикардию, существенно падает артериальное давление (АД).
В этой фазе перкуссионные методы исследования выявляют притупленный перкуторный звук, в основном в задненижних отделах, аускультативно обнаруживается жесткое дыхание, иногда и сухие хрипы. Если обнаружены влажные хрипы и крепитация, это говорит о появлении жидкости в альвеолах, что называется в медицине альвеолярным отеком легких, который может быть как незначительно, так и сильно выраженным. Рентгенография легких показывает выраженный интерстициальный отек легких, а также двусторонние инфильтративные тени неправильной облаковидной формы, сливающиеся с корнями легких и друг с другом. Часто в краевых отделах средней и нижней долей на фоне усиленного сосудистого рисунка появляются очаговоподобные тени. В этом периоде сильно снижается РаО2 — 50 мм рт.ст., даже если проводится ингаляция О2.
Четвертый период называется терминальным. В нем сильно прогрессирует дыхательная недостаточность, развивается выраженная артериальная гипоксемия и гиперкапния, метаболический ацидоз. Формируется острое легочное сердце по причине нарастающей легочной гипертензии. IV период респираторного дистресс-синдрома взрослых характеризуется такой симптоматикой:
- профузная потливость
- выраженная одышка и цианоз
- резкое падение артериального давления вплоть до коллапса
- глухость сердечных тонов тахикардия, часто также различные аритмии
- влажные хрипы в большом количестве (разного калибра) в легких, обильная крепитация
- кашель с пенистой мокротой розового оттенка
В этой стадии развиваются признаки усиливающейся легочной гипертензии и синдрома острого легочного сердца. На легочной артерии фиксируют расщепление и акцент II тона. Среди ЭКГ признаков стоит отметить выраженное отклонение электрической оси сердца вправо, высокие остроконечные зубцы Р в отведениях II, III, avF, V1-2. Рентгенограмма обнаруживает признаки повышения давления в легочной артерии, выбухание ее конуса.
Для четвертой стадии синдрома типично развитие полиорганной недостаточности. Нарушается функционирование почек, потому проявляются:
- протеинурия
- олигоанурия
- микрогематурия
- цилиндрурия
- повышением содержания в крови мочевины
- повышением содержания в крови креатинина
Функция печени также нарушается, потому появляется легкая желтушность, сильно повышается количество в крови фруктозо-1-фосфаталь-долазы, аланиновой аминотрансферазы и лактатдегидрогеназы. Нарушается функция головного мозга: больной становится заторможенным, наблюдаются головокружения, головные боли, могут быть симптомы нарушения мозгового кровообращения. При исследовании газового состава крови фиксируют гиперкапнию и глубокую артериальную гипоксемию. Проводят исследование кислотно-щелочного равновесия, которое выявляет метаболический ацидоз.
Диагноз и рекомендуемые клинические исследования
Для РДС характерна появляющаяся в первые 6 ч после родов триада рентгенологических признаков: диффузные очаги пониженной прозрачности, воздушная бронхограмма, уменьшение воздушности легочных полей.
Эти распространенные изменения наиболее отчетливо выявляются в нижних отделах и на верхушках легких. Помимо этого заметны уменьшение объема легких, кардиомегалия различной степени выраженности. Нодозно-ретикулярные изменения, отмечающиеся при рентгенологическом исследовании, по мнению большинства авторов, представляют собой рассеянные ателектазы.
Для отечно-геморрагического синдрома типичны «размытая» рентгенологическая картина и уменьшение размеров легочных полей, а клинически — выделение пенистой жидкости с примесью крови изо рта.
Если указанные признаки не выявляются при рентгенологическом исследовании спустя 8 ч после родов, то диагноз РДС представляется сомнительным.
Несмотря на неспецифичность рентгенологических признаков, проведение исследования необходимо для исключения состояний, при которых иногда требуется хирургическое вмешательство. Рентгенологические признаки РДС исчезают спустя 1—4 недели в зависимости от тяжести заболевания.
Рекомендуемые методы исследования:
■ рентгенологическое исследование грудной клетки;
■ определение показателей КОС и газов крови;
■ общий анализ крови с определением числа тромбоцитов и вычислением лейкоцитарного индекса интоксикации;
■ определение гематокрита;
■ биохимический анализ крови;
■ УЗИ головного мозга и внутренних органов;