Респираторный дистресс-синдром взрослых: причины, симптомы, лечение
Содержание:
- Причины
- Признаки
- Патогенез
- Общие сведения
- Почему этот синдром особенно часто встречается при COVID-19
- Справиться с ОРДС очень непросто
- Как это описал врач
- С этим синдромом есть еще одна проблема, которая делает новый коронавирус особенно опасным
- Как лечится острый респираторный дистресс-синдром?
- Виды
- Диагноз и рекомендуемые клинические исследования
- История и физика
- Своеобразная история этой новой болезни
- Патологические изменения.
- Патогенез
- Клиническое обследование
- Диагностика
Причины
Среди причин развития ОРДС у взрослых выделяют легочные (прямые) и внелегочные (непрямые) повреждающие факторы:
- К легочным факторам относятся: ушибы/травмы легких, инфекционно-воспалительные заболевания легких, пневмоторакс, аспирация жидкости, радиационный пневмонит, легочное кровотечение, тромбоэмболия легочной артерии, отравление токсическими газами, трансплантация легкого.
- К внелегочным факторам относятся: массивная гемотрансфузия, сепсис, ожоги, тяжелые неторакальные травмы, шок, передозировка лекарств/наркотических средств, обширные оперативные вмешательства, уремия, ДВС-синдром, онкозаболевания, панкреонекроз, системные патологии, сильное переохлаждение/перегревание организма, электротравма, утопление.
К основным причинам развития РДС у новорожденных относятся:
- нарушение процесса выработки/экскреции сурфактанта альвеолоцитами, обусловленное структурной/функциональной незрелостью тканей легких;
- врожденный (генетически обусловленный) дефект структуры сурфактанта.
Предрасполагающими факторами развития РДС у ребенка являются:
- дистресс плода, обусловленный различными негативными внутриутробными факторами (внутриутробная гипоксия, гемолитическая болезнь плода, асфиксия в родах, преждевременная отслойка плаценты и др.);
- пневмопатия у новорожденных (морфофункциональная незрелость тканей легких, аспирация околоплодных вод, ателектазы легких, отечно-геморрагический синдром и др.);
- преждевременные роды/кесарево сечение при отсутствии родовой деятельности;
- сахарный диабет 1-го типа у матери;
- недоношенность;
- асфиксия новорожденного;
- охлаждение ребенка, гиповолемия.
Признаки
Дистресс в психологии острого характера – это патология, которую заметить невозможно. Распознать возможно только хроническую форму.
Она выражается:
- появлением у человека вредных привычек;
- изменением вкусовых предпочтений;
- снижением или, наоборот, ростом аппетита;
- изменением характера;
- потерей интереса к любимым делам;
- отсутствием стремления к улучшению своей жизни, равнодушием ко всему окружающему;
- нарушением работы нервной системы, беспокойством, бессонницей, снижением работоспособности;
- ухудшением мыслительного процесса;
- головными болями, повышением артериального давления, ознобом, тошнотой;
- изменением речи. Человек начинает заикаться, проглатывать фразы, произносить слова неясно.
Проявление дистресса сопровождается 4 основными моделями поведения:
- Паническим страхом – он не может быть объяснен логически, индивид теряет способность правильно реагировать на сложившуюся ситуацию.
- Агрессия и гнев и по отношению к окружающим, и к себе лично. Такое поведение мешает подобрать компромисс.
- Стремление уйти от реальности.
- Зацикливание на проблеме.
Синдром дистресса является одной из главных причин развития ишемической болезни сердца и гипертонии.
Патогенез
Этиологические (причинные) факторы приводят к тому, что в интерстициальной ткани легких и в капиллярах органа собираются активированные лейкоциты и тромбоциты в большом количестве. Исследователи выдвигают предположение, что происходит выделением ими множества биологически активных веществ:
- простаглавдинов
- протеиназ
- лейкотриенов
- токсических кислородных радикалов и т.д.
Они повреждают альвеолярный эпителий и эндотелий сосудов, меняют реактивность сосудов, тонус бронхиальной мускулатуры, способствуют развитию фиброза. Выше перечисленные биологические вещества оказывают влияние на повреждение альвеолярного эпителия и эндотелия капилляров легких. За короткий промежуток времени увеличивается проницаемость сосудов, происходит спазм легочных капилляров, повышается давление внутри них. Фиксируется выраженное пропотевание плазмы и эритроцитов в альвеолы и интерстициальную ткань легких, развивается отек легких и ателектаз. Также на развитие ателектаза влияет вторичное снижение активности сурфактанта.
Выше описанные процессы влияют на главные патофизиологические механизмы:
- шунтирование венозной крови в артериальное русло
- гиповентиляция альвеол
- нарушение диффузии кислорода и углекислого газа
- нарушение соответствия между вентиляцией и перфузией
Общие сведения
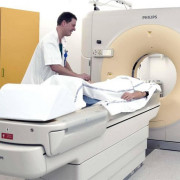
Острый респираторный дистресс-синдром у взрослых (син. некардиогенный отек легких) представляет собой остро возникающее проявление дыхательной недостаточности, обусловленное диффузным воспалением паренхимы легких, которое развивается в виде неспецифической реакции на повреждающие агрессивные факторы различного генеза, приводящие к развитию некардиогенного отека легких с проявлением острой дыхательной недостаточности. Встречается острый респираторный дистресс-синдром (ОРДС) как у взрослых, так и у детей. Распространенность ОРДС колеблется в пределах 57-62 случая/100 тыс. населения/год, а показатели летальности зависят от этиологического фактора, тяжести течения/полиорганной недостаточности и могут варьировать от 16 до 82%.
В основе ОРДС взрослых, несмотря на его полиэтиологичность лежат патологические процессы, приводящие к повреждениям/изменению структур легочной ткани (альверно-капилярной мембраны), вызывающие нарушение проходимости мелких дыхательных путей и соответственно, несостоятельность транспортировки кислорода в легкие. Является частым осложнением различных заболеваний, отравлений, травм; наиболее часто ОРДС развивается при синдроме полиорганной недостаточности/системного воспалительного ответа. Быстро нарастающее снижение оксигенации/вентиляции организма вызывает развитие критических для жизни состояний, обусловленных кислородной недостаточностью головного мозга/сердца. Несмотря на существующую тенденцию к снижению показателей летальности, ОРДС остается важнейшей проблемой интенсивной терапии и современной пульмонологии. Респираторный дистресс синдром взрослых относится к критическим состояниям, требующим экстренной оценки состояния пациента и оказания неотложной помощи.
Респираторный дистресс синдром у детей (син. болезнь гиалиновых мембран, синдром дыхательных расстройств). Развивается у детей в первые дни жизни, то есть это патология новорожденных детей, обусловленная первичным нарушением образования (дефицитом) сурфактанта и функциональной/структурной незрелостью легких. Это способствует снижению эластичности ткани легкого, спаданию альвеол и развитию диффузных ателектазов, что проявляется резко выраженной дыхательной недостаточностью у ребенка уже в первые часы после рождения. Без немедленного лечения неизбежно развивается полиорганная недостаточность, приводящая к смерти ребенка.
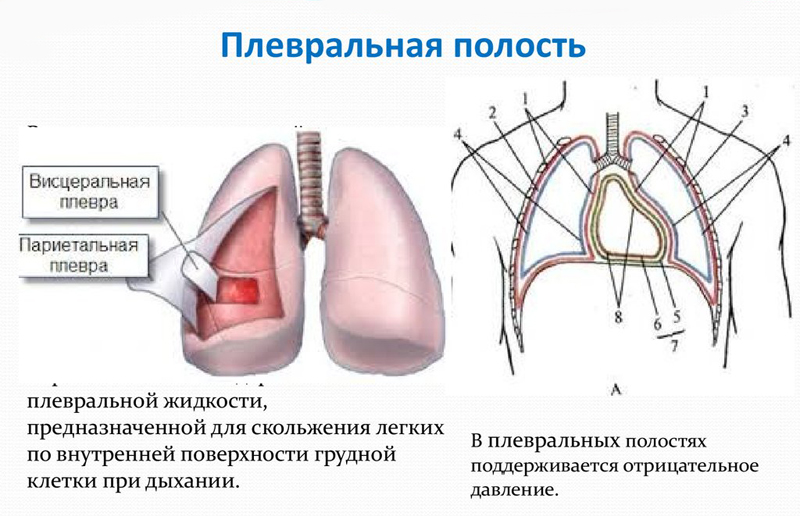
Сурфактант представляет собой смесь поверхностно-активных веществ, покрывающих изнутри лёгочные альвеолы, основной функцией которых является недопущение спадения стенок альвеол за счет снижения поверхностного натяжения. В период внутриутробного развития плода синтез альвеолоцитами II типа сурфактанта начинается с 25-26 недели, но наиболее интенсивный процесс происходит начиная с 33-34 недели и на 35-36-й неделе гестации к моменту родов полностью завершается, что и способствует первичному расправлению легких. То есть, количество сурфактанта в легких обратно коррелирует с гестационным возрастом новорожденного. Созревание системы сурфактанта происходит под влиянием различных гормонов (кортизол, адреналин/норадреналин, гормоны щитовидной железы, эстрогены, катехоламины).
Синдром дыхательных расстройств у новорожденных — это самостоятельная нозологическая форма (МКБ-10: Р22.0). Иногда встречается термин этого заболевания «болезнь гиалиновых мембран» возникший по причине отложения гиалиноподобного вещества на внутренней поверхности альвеол/респираторных бронхиол. Частота возникновения возрастает по мере уменьшения гестационного возраста/массы тела ребенка при рождении.
Респираторный дистресс синдром новорожденных (РДС) относится к наиболее часто встречаемым/тяжелым заболеваниям недоношенных детей. На него приходится порядка 27% среди всех умерших детей, а у новорожденных детей, которые родились на 26-28 неделях гестации, этот показатель достигает 75%. Его встречаемость варьирует от 80 % у детей, рожденных на сроке гестации до 27 недель и 5-10% у рожденных на сроке гестации 35-36 недель. У доношенных детей синдром дыхательных расстройств возникает в 2-2,6% случаев и обусловлен преимущественно асфиксией в родах и морфофункциональной незрелостью ткани легких.
Почему этот синдром особенно часто встречается при COVID-19
Новый коронавирус умеет в клетки дыхательных путей, альвеол, сосудов, сердца, почек и желудочно-кишечного тракта. Хотя легкие все же страдают больше всего. Пораженные клетки производят множество копий коронавируса и в итоге погибают. Все это запускает и поддерживает воспалительный ответ иммунной системы.
В норме сама иммунная система со временем подавляет это воспаление, и человек выздоравливает. Но при инфицировании коронавирусом чаще, чем во многих других случаях, бывает, что тормозящие механизмы иммунной системы не срабатывают как надо. В худшем варианте развития событий это приводит к состоянию под названием «цитокиновый шторм». Тогда захватывается весь организм, и могут поражаться даже почки и сердце. И, конечно, кроме прочего, развивается ОРДС. Другими словами, в масштабных повреждениях может принимать участие уже не вирус, который запустил агрессивный ответ, а непосредственно иммунная система человека, которая вышла из-под контроля.
Справиться с ОРДС очень непросто
При ОРДС по-хорошему нужно решить две задачи: добиться того, чтобы уровень насыщения крови кислородом был достаточным и чтобы иммунная система перестала уничтожать легкие. Первая проблема изучена лучше второй, и решения там, можно сказать, есть.
Насыщение крови кислородом
Острый респираторный дистресс-синдром не всегда означает, что за человека дышит аппарат искусственной вентиляции легких (ИВЛ). На самом деле в определенных условиях можно обойтись другими методами, хотя все же стандартная тактика — ИВЛ. Правда, не всегда аппарат именно дышит за человека: бывает, он работает во вспомогательном режиме. Оставлять человека без такой помощи в надежде, что организм справится сам, довольно опасно. Кроме того, если человек умрет, то смерть его, вполне вероятно, будет мучительной.
Как это описал врач
Из поста нью-йоркского реаниматолога Евгения Пинелиса:
«ИВЛ — поддерживающая терапия. Альтернатива ей — смерть от удушья.
Это не слишком честный полемический ход, но я могу. Вы видели, как умирают от удушья? <…> Я — видел. И помнить буду всегда и всех. Пациент с терминальной стадией фиброза легких, которому ИВЛ действительно был противопоказан, так как он не мог получить легочный трансплантат. Пожилые люди с тяжелой пневмонией, которые сами выбрали отказаться от вентиляции. Морфий помогает, но не полностью. И его надо ждать из аптеки. И видеть дыхание по сорок пять раз в минуту (попробуйте просто), синеющие губы, бред или ужас.
Во время эпидемии COVID-19 все мы видели это десятки раз. Пациенты, вырывающиеся из рук врачей и медсестер и сдирающие с себя кислородные маски. Или просто сконцентрированные только на дыхании. На всех этих 45 вдохах и выдохах. За шестьдесят секунд. Когда вместе с диафрагмой работает все тело, кажется иногда, что даже икроножные мышцы».
Если стандартная версия ИВЛ не помогает, человека могут положить на живот, продолжая вентиляцию легких (это предлагает и Всемирная организация здравоохранения). Так, , перераспределяется кровоток в легких, и кровь протекает по тем участкам, в которых кислород может в нее попасть.
При тяжелом ОРДС еще используют препараты для нейромышечной блокады и — редко — оксид азота. Хотя польза от этих препаратов вызывает споры.
В крайнем случае можно использовать экстракорпоральную мембранную оксигенацию (ЭКМО), то есть пропускать кровь пациента через аппарат, который обогащает ее кислородом, забирает углекислый газ и возвращает ее человеку. Но такие аппараты редки и требуют большого количества специально обученного персонала. Кроме того, эффективность ЭКМО при новой коронавирусной инфекции под сомнением, хотя Всемирная организация здравоохранения предлагает рассмотреть такой вариант.
Налаживание работы иммунной системы
Что касается работы иммунной системы, сейчас есть средства, которые, предположительно, могут сработать точечно и повлиять на нужные механизмы. Но, как обычно бывает в случае COVID-19, достаточно хороших исследований еще нет. При похожих состояниях — когда иммунная система ведет себя агрессивно — иногда назначаются некоторые моноклональные антитела (например, тоцилизумаб). Они могут снижать уровень веществ, участвующих в процессе воспаления. Есть небольшие работы, которые показывают эффективность тоцилизумаба, но пока нет по-настоящему надежных исследований, которые бы показывали эффективность этого подхода при новой коронавирусной инфекции. По всей видимости, если он и работает, то в тяжелых случаях, но при этом до развития ОРДС.
Более грубое вмешательство может привести к распространению вируса. Поэтому, например, глюкокортикоиды, которые подавляют работу иммунной системы, использовать только в крайних случаях, и то не все организации.
С этим синдромом есть еще одна проблема, которая делает новый коронавирус особенно опасным
Даже если человек пережил ОРДС, это не значит, что он станет прежним и в психическом, и в физическом смысле. Примерно у 40% бывших пациентов в той или иной степени нарушается мышление. Возможно, это связано с тем, что какое-то время мозг получал недостаточно кислорода. У таких людей чаще бывают депрессия, тревога и посттравматическое стрессовое расстройство. Части из них сложнее выдерживать прежние физические нагрузки, а легкие обычно работают хуже, чем раньше.
Как лечится острый респираторный дистресс-синдром?
ОРДС является серьезным и опасным для жизни состоянием, которое требует лечения в отделении интенсивной терапии, где имеется соответствующая респираторная и кровеносная поддержка. Лечение будет сосредоточено на:
- Выявление и лечение первопричины. Если подозреваемой (гной образующие бактерии или их токсины в крови и тканях), следует начинать антибиотикотерапию с применением антибиотиков широкого спектра действия. Другие состояния, такие как травма, будут лечиться надлежащим образом.
- Предотвращение осложнений лечения. Осторожные методы искусственной вентиляции легких должны предотвратить развитие пневмонии и других травм легких, индуцированных этой болезнью.
- Поддерживающий уход. Большинству пациентов требуется кислород и вентиляция, чтобы достаточное количество кислорода могло попасть в легкие и сохранить дыхательные пути открытыми. Поддержка кровообращения включает в себя тщательное управление жидкостью (сокращение потребления жидкости для удаления избытка жидкости из легких), переливание крови и приём медикаментов, помогающих расширить сосуды и улучшить прокачку тепла. Все это помогает сердцу поддерживать адекватную работу. Пищевая поддержка необходима больным с тяжелым случаем заболевания, вам также может потребоваться питание через гастростому (вставная трубка для кормления). Диализ может потребоваться при почечной недостаточности.
- Прочие методы терапии. При лечении ОРДС был испытан ряд других средств, включая закись азота (которая расширяет сосуды в легких), поверхностно-активное вещество (жидкость, удерживающая дыхательные пути открытыми) и терапию стероидами. Но большинство из них не смогли показать хорошие результаты в плане выживаемости больных пациентов. Однако, стероиды могут использоваться на более поздних стадиях заболевания для ускорения выздоровления путем уменьшения воспаления.
Виды
Стрессовые нагрузки могут действовать на человека с различной длительностью.
В зависимости от этого фактора выделяются две формы дистресса:
| Наименование | Характеристики |
| Острый | Это внезапное событие, которое было совершенно неожиданно для человека. Стремительность привела к развитию шокового состояния. Чаще всего это крупные происшествия, которые стали угрозой для жизни самого индивида или близких. Например, катастрофа, несчастный случай, тяжелая болезнь. При остром виде дистресса может наблюдаться неадекватная реакция со стороны человека. Он может начать совершать непонятные поступки, начать употреблять наркотики или спиртные напитки. Острый вид патологии часто отражается на состоянии здоровья. Например, у человека развивается гипертонический криз, инфаркт или инсульт. |
| Хронический | Такой вид характеризуется кардинальным изменением поведения человека из-за воздействия на него длительных стрессовых ситуаций. Это могут быть конфликты в семье или на работе, тяжелое заболевание. |
Дистресс не только сам влияет на ухудшение состояния здоровья, но и развивается активнее, если у человека есть хронические заболевания. Быстрее всего в стадию дистресса впадают люди с гормональными нарушениями, сердечно-сосудистыми и гинекологическими проблемами.
Диагноз и рекомендуемые клинические исследования
Для РДС характерна появляющаяся в первые 6 ч после родов триада рентгенологических признаков: диффузные очаги пониженной прозрачности, воздушная бронхограмма, уменьшение воздушности легочных полей.
Эти распространенные изменения наиболее отчетливо выявляются в нижних отделах и на верхушках легких. Помимо этого заметны уменьшение объема легких, кардиомегалия различной степени выраженности. Нодозно-ретикулярные изменения, отмечающиеся при рентгенологическом исследовании, по мнению большинства авторов, представляют собой рассеянные ателектазы.
Для отечно-геморрагического синдрома типичны «размытая» рентгенологическая картина и уменьшение размеров легочных полей, а клинически — выделение пенистой жидкости с примесью крови изо рта.
Если указанные признаки не выявляются при рентгенологическом исследовании спустя 8 ч после родов, то диагноз РДС представляется сомнительным.
Несмотря на неспецифичность рентгенологических признаков, проведение исследования необходимо для исключения состояний, при которых иногда требуется хирургическое вмешательство. Рентгенологические признаки РДС исчезают спустя 1—4 недели в зависимости от тяжести заболевания.
Рекомендуемые методы исследования:
■ рентгенологическое исследование грудной клетки;
■ определение показателей КОС и газов крови;
■ общий анализ крови с определением числа тромбоцитов и вычислением лейкоцитарного индекса интоксикации;
■ определение гематокрита;
■ биохимический анализ крови;
■ УЗИ головного мозга и внутренних органов;
История и физика
Клинический спектр COVID-19 варьируется от бессимптомных или малосимптомных форм до клинических состояний, характеризующихся дыхательной недостаточностью, требующей искусственной вентиляции легких и поддержки в отделении интенсивной терапии, до полиорганных и системных проявлений в виде сепсиса, септического шока и синдромов полиорганной дисфункции (MODS).
В одном из первых сообщений о заболевании ученый Huang показал, что пациенты страдали лихорадкой, недомоганием, сухим кашлем и одышкой. Компьютерная томография (КТ) грудной клетки показала пневмонию с отклонениями от нормы во всех случаях. Около трети из них (13, 32%) требовали помощи в отделении интенсивной терапии. В итоге было зафиксировано 6 (15%) смертельных случаев.
Тематические исследования ещё одного ученого Li, опубликованные в Медицинском журнале Новой Англии (NEJM) в январе 2020 г., охватили первые 425 случаев, зарегистрированных в Ухане. Данные показывают, что средний возраст пациентов составлял 59 лет с диапазоном от 15 до 89 лет. Таким образом, они не сообщали о клинических случаях у детей младше 15 лет. Существенных гендерных различий не было – 56% составили мужчины. В последующих отчетах отмечается меньшая распространенность женского пола.
Клинические и эпидемиологические данные Китайского центра контроля заболеваний и данные о 72 314 историях болезни (подтвержденных, предполагаемых, диагностированных и бессимптомных случаев) были опубликованы в Журнале Американской медицинской ассоциации (JAMA), что стало первой важной иллюстрацией эпидемиологической кривой Китая. Во время вспышки было 62% подтвержденных случаев, в том числе 1% случаев, которые были бессимптомными, но были лабораторно-положительными (тест на вирусную нуклеиновую кислоту). . Кроме того, общая летальность (по подтвержденным случаям) составила 2,3%
Следует отметить, что погибли в основном пациенты пожилого возраста, особенно в возрасте ≥ 80 лет (около 15%) и от 70 до 79 лет (8,0%). Приблизительно половина (49,0%) погибших пациентов страдали от ранее существовавших сопутствующих заболеваний, таких как сердечно-сосудистые заболевания, диабет, хронические респираторные заболевания и онкологические заболевания. 1% пациентов были в возрасте 9 лет и младше, но смертельных случаев в этой группе не было
Кроме того, общая летальность (по подтвержденным случаям) составила 2,3%. Следует отметить, что погибли в основном пациенты пожилого возраста, особенно в возрасте ≥ 80 лет (около 15%) и от 70 до 79 лет (8,0%). Приблизительно половина (49,0%) погибших пациентов страдали от ранее существовавших сопутствующих заболеваний, таких как сердечно-сосудистые заболевания, диабет, хронические респираторные заболевания и онкологические заболевания. 1% пациентов были в возрасте 9 лет и младше, но смертельных случаев в этой группе не было.
Авторы отчета китайского CDC разделили клинические проявления заболевания по степени тяжести:
- Легкое заболевание: не пневмония и легкая пневмония – 81% случаев.
- Тяжелое заболевание: одышка, частота дыхания ≥ 30 / мин, сатурация крови кислородом (SpO2) ≤ 93%, соотношение PaO2 / FiO2 или P / F <300 и / или инфильтраты легких> 50% в течение 24-48 часов – 14% случаев.
- Критическое заболевание: дыхательная недостаточность, септический шок и / или полиорганная дисфункция (MOD) или недостаточность (MOF) – 5% случаев.
Согласно последующим отчетам, у 70% пациентов заболевание протекает бессимптомно или с очень легкими симптомами, в то время как у оставшихся 30% наблюдается респираторный синдром с высокой температурой, кашлем до достижения тяжелой дыхательной недостаточности.
Таким образом, данные, полученные из отчетов и директив органов здравоохранения, позволяют разделить клинические проявления болезни в зависимости от степени тяжести клинических картин. COVID-19 может проявляться в легкой, средней или тяжелой форме. Среди тяжелых клинических проявлений – тяжелая пневмония, ОРДС, а также внелегочные проявления и системные осложнения, такие как сепсис и септический шок.
Клиническое течение болезни, по-видимому, предсказывает благоприятную тенденцию у большинства пациентов. В некотором количестве случаев, процентную составляющую которых еще предстоит определить, примерно через неделю происходит внезапное ухудшение клинических состояний с быстро ухудшающейся дыхательной недостаточностью и MOD / MOF. В качестве ориентира можно использовать критерии степени тяжести дыхательной недостаточности и диагностические критерии сепсиса и септического шока.
Своеобразная история этой новой болезни
У некоторых пациентов клиническая история этого заболевания имеет определенные особенности.
- Предполагается, что у пациента, прежде всего, будет лихорадка, которая плохо поддается лечению жаропонижающими средствами, и состояние недомогания. Часто сопровождается сухим кашлем.
- Через 5-7 дней пожилые пациенты с уже нарушенной функцией легких начинают испытывать одышку и учащение дыхания. Однако у более слабых пациентов одышка может появиться уже при появлении симптомов. С другой стороны, у более молодых людей и у тех, у кого нет основных респираторных нарушений или других сопутствующих заболеваний, одышка может появиться позже.
- У пациентов с ухудшением вызванным воспалительным поражением легких, наблюдается снижение насыщения кислородом (<93%). Похоже, что это критическая фаза болезни, начиная с этого момента, возможно быстрое ухудшение дыхательной функции.
Сценарий поистине невероятен, потому что для пациентов с малосимптомными и слегка гипоксическими заболеваниями первым терапевтическим подходом является кислородная терапия. Хотя эта стратегия эффективна, у некоторых пациентов может наблюдаться обострение дыхательной недостаточности.
Следующим шагом, согласно логике, будет NIV. Эта терапия имеет быстрый успех за счет увеличения P / F. Однако у некоторых пациентов наблюдается внезапное и неожиданное ухудшение клинического состояния. Пациенты теряют сознание и требуют быстрой интубации и инвазивной механической вентиляции.
Патологические изменения.
Патологические изменения в легких, выявляемые при РДСВ, оказываются сходными вне зависимости от конкретного этиологического
фактора, что доказывает справедливость известного положения о том, что легкие
«отвечают» на самые различные повреждающие воздействия достаточно ограниченным,
стереотипным набором патологических изменений. Как правило, легкие отечны,
безвоздушны, с участками геморрагии, ателектазов и уплотнений. При световой
микроскопии выявляют отек и клеточную инфильтрацию межальвеолярных перегородок и
интерстициального пространства, окружающего воздухоносные пути, а также
гиалиновые мембраны во многих участках легких, стаз эритроцитов, тромбоцитарные
и гранулоцитарные агрегаты в очагах альвеолярных и интерстициальных геморрагии.
Нередко при этом отмечают гиперплазию и дисплазию гранулярных пневмонитов.
Если длительность течения РДСВ составляет более 10 сут, то в дополнение к
вышеприведенным морфологическим «находкам» обнаруживают фиброз легочной ткани. В
случаях выздоровления или смерти в последующем от какой-либо другой причины в
легких выявляют выраженный интерстициальный фиброз и эмфизематозные изменения.
Впрочем, при адекватном лечении значительная часть больных полностью
выздоравливает и при последующем проспективном наблюдении у них не отмечают
каких-либо нарушений со стороны дыхательной системы.
Патогенез
Микрофотография диффузного поражения альвеол при ОРДС. Окраска гематоксилином и эозином.
В основе ОРДС лежит диффузное воспаление лёгких. В этом процессе выделяют 3 фазы: экссудативная, пролиферативная и фибротическая.
В экссудативную фазу в ответ на воспаление выделяются цитокины и другие провоспалительные вещества, которые активируют альвеолярные макрофаги и циркулирующие нейтрофилы. В свою очередь, активированные нейтрофилы прикрепляются к эндотелию лёгочных капилляров и высвобождают содержимое своих цитоплазматических гранул (протеазы и токсические метаболиты кислорода). Это приводит к повреждению эндотелия капилляров и эпителия альвеол, нарушая альвеолярно-капиллярный барьер. В результате экссудат проникает в лёгочную паренхиму и альвеолярное воздушное пространство. Нарушается газообмен и возникает гипоксия. Также возможно повреждение альвеолоцитов II типа, которые отвечают за образование сурфактанта. При этом происходит спадение альвеол, снижение растяжимости лёгких и внутрилёгочное шунтирование. Кроме того, развивается лёгочная гипертензия в результате внутрисосудистой обструкции тромбами, спазма лёгочных сосудов из-за гипоксии и действия некоторых воспалительных медиаторов (тромбоксан, лейкотриены и эндотелин).
В пролиферативную фазу у большинства пациентов происходит восстановление лёгких: удаляется экссудат, нейтрофильная инфильтрация сменяется лимфоцитарной. Пролиферируют альвеолоциты II типа, которые образуют новый сурфактант и дифференцируются в альвеолоциты I типа. Но несмотря на такие улучшения, у многих больных сохраняется одышка, тахипноэ, гипоксемия. У некоторых пациентов процесс переходит в фибротическую фазу. Накопленный в лёгких фибрин подвергается ремоделированию и может вызывать фиброз.
Клиническое обследование
Для диагностики ОРДС врач будет искать ряд клинических признаков, которые имеют острое начало. Врач проверит вашу общую внешность, внимательно выслушает вашу грудь и проверит насыщение кислородом с помощью кислородного зонда на пальце.
Некоторые признаки ОРДС, которые врач будет искать, включают:
- цианоз (синеватая окраска, локализирующаяся на языке, губах);
- тахипноэ (учащенное, поверхностное дыхание);
- тахикардия сердца (учащение пульса);
- усиление гипоксемии (низкие концентрации кислорода в крови);
- периферическая вазодилатация (открытие кровеносных сосудов на периферии вашего тела);
- хрипы в груди: врач прослушает вашу грудную клетку с помощью стетоскопа, чтобы услышать хрипящие, скрипучие или потрескивающие звуки, которые указывают, что ваше воздушное пространство не работает должным образом.
Как диагностируется ОРДС?
Если у вас есть подозрения на наличие ОРДС, врач проведет ряд различных анализов. Общий анализ крови, функции почек, функции печени (печеночная проба, LFT), анализ свертываемости крови и посев крови — все это необходимо. Эти исследования могут помочь определить, есть ли у вас предрасполагающая инфекция, вероятные ошибки и дать врачу представление о том, насколько хорошо функционируют другие ваши органы.
Рентгенография грудной клетки является чрезвычайно важным инструментом в диагностике и мониторинге прогрессирования заболевания. При исследовании врач может визуализировать накопление жидкости в легких.
Вы также будете регулярно измерять концентрацию кислорода в крови, а также можете провести другие более специализированные исследования, такие как введение специальных катетеров (тонких трубок) для измерения определенного артериального давления. Это исключает другие причины накопления жидкости в легких, такие как застойная сердечная недостаточность.
Диагностика
Клинические проявления респираторного дистресс-синдрома у взрослых не являются специфическими (то есть, проявляются не только при данном состоянии). Поэтому для подтверждения диагноза потребуются физикальное исследование (ощупывание грудной клетки, которое выявит нарастание жесткости и неэластичности ее элементов, простукивание и выслушивание фонендоскопом), а также дополнительные методы диагностики – инструментальные и лабораторные.
Из инструментальных методов самые информативные – это:
- рентгенография легких;
- электрокардиография.
Из лабораторных методов диагностики показательными при респираторном дистресс-синдроме являются следующие:
- общий анализ крови;
- общий анализ мочи;
- определение газового состава крови с измерением парциального давления кислорода и углекислого газа;
- исследование кислотно-щелочного баланса (pH артериальной крови составляет ниже 7,3).
В первом периоде дистресс-синдрома изменения при инструментальных и лабораторных исследованиях выявлены не будут.
Во втором периоде изменяется рентгенологическая картина – сосудистый рисунок легких более выраженный, особенно в отделах легкого, более отдаленных от его корня. Это свидетельствует о начавшемся отеке легкого. Газовый состав крови или не изменен, или выявляется несущественное снижение парциального давления кислорода.
В третьем периоде на рентген-снимке видно выбухание легочной артерии (из-за повышения давления в ней), а ЭКГ продемонстрирует перегрузку правых отделов сердца.
В четвертом периоде во время рентгенографии и электрокардиографии будут выявлены признаки сильно перегруженных правых отделов сердца – фактически это признаки легочного сердца (состояния, когда из-за перегрузки расширены правые отделы сердца). В крови обнаруживают критическое нарастание количества углекислого газа и прогрессирующее снижение количества кислорода.
- креатинина;
- мочевины.
В моче будут выявлены:
- протеинурия (выделение белка с мочой);
- микрогематурия (кровь в моче, которая при визуальном осмотре не определяется, но ее можно выявить при исследовании мочи под микроскопом);
- цилиндрурия (выделение с мочой цилиндров – специфических слепков из слущенных эпителиальных клеток, эритроцитов, лейкоцитов и частичек жира).
Повреждение печени в рамках полиорганной недостаточности фиксируют на основании значительного повышения в крови некоторых ферментов печени, которые высвобождаются в кровь по причине разрушения ее клеток (это аланинаминотрансфераза и лактатдегидрогеназа).