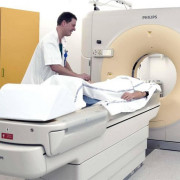
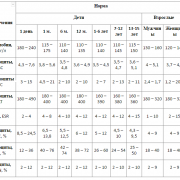
Важность процесса гемопоэза и схема гемопоэза в жизни человека
Содержание:
- Микроскопическая. Ультраструктурная и цитохимическая характеристика клеток в дифферонах эритроцитов, гранулоцитов, моноцитов, т-, влимфоцитов и тромбоцитов.
- Как осуществляется кроветворение: механизмы
- Особенности дифференцировки гемопоэтических клеток
- Регуляция кроветворения
- Что будет, если гемопоэз нарушится
- Васкуляризация. Иннервация. Возрастные изменения. Регенерация.
- Что такое гемопоэз и последствия его нарушений
- Особенности процесса образования клеток крови: теории и факты
- Постэмбриональный гемопоэз
- Назначение схемы гемопоэза
- Роль витамина В12 в кроветворении
- Гемопоэтическая стволовая клетка
- Контроль гемоцитопоэза
- Что представляет собой процесс кроветворения и где он происходит
- Регуляция гемопоэза
Микроскопическая. Ультраструктурная и цитохимическая характеристика клеток в дифферонах эритроцитов, гранулоцитов, моноцитов, т-, влимфоцитов и тромбоцитов.
эритроциты:
стволовая
кроветворная клетка
—
полустволовая
(полустволовая
клетка предшественница )-
бурстобразующая
-э(быстро делятся и форм колонии
клеток)-кое-э(делятся менее активно,
высокая акт к эритропоэтину)-проэритробласт(накапл
рибосомы-базофилия, накапл гемоглобин,
который обеспечивает оксифилию)-полихроматофильные
эритробласты(полихроматофилия за счет
накопления гемоглобина (оксифилия) и
наличия рибосом(базофилия))-оксифильные
эритробласты( преобл гемоглобина, быстро
теряют способность к делению, теряют
ядро)-ретикулоциты(нет ядра)-эритроциты.
Гранулоциты:
скк-пск(кое-гэмм)-кое-гм—кое-Гн,эо,б—миелобласты—промиелоциты(образование
органелл белкового синтеза, секреция
первичных гранул)—миелоциты(секреция
первичных и вторичных гранул, накопление
органелл, изменение структуры
ядра)—метамиелоциты(секреция третичных
гранул, дальнейшие изм ядра)—палочкоядерные
и сегментоядерные гранулоциты( изменение
ядра, органелл белкового синтеза,
накопление третичных гранул).
Тромбоциты:скк-пск(кое-гэмм)—кое-Мкц—мегакариобласт(большая,крупное
ядро)—промегакариоцит—мегакариоцит(накопление
гранул, тесный контакт с синусоидным
капилляром)—тромбоцит(образыется путем
отщепления цитоплазмы от мегакариоцита).
Моноциты:скк-пск(кое-гэмм,ГМ)—кое-м—монобласт—промоноцит—моноцит—в
кровь—в соед ткань—макрофаг. Происходит
увеличение клетки, накопление лизосом,
формир антигенного состава.
Лимфоцитопоэз:
скк—кое-л—про-В(Т)-лимфоциты—пре-пре-В-лимфоциты—пре-В(Т)-лимфоцит—незрелый
В(Т)-лимфоцит—зрелый
Происходит
уменьшение размера клеток, изменение
ядра
Как осуществляется кроветворение: механизмы
Процессы разрушения красных кровяных шариков и их образования строго сбалансированы. Если организм теряет какое-то количество крови, то не проходит 2—3 недель, как снова восстанавливается исходный уровень числа эритроцитов и концентрации гемоглобина. При этом всегда наблюдается значительное убыстрение образования красных кровяных телец (эритропоэза) в костном мозге.
Не вызывает сомнений факт существования в организме особых механизмов регуляции эритропоэза, хорошо выявляемых тогда, когда под влиянием каких-либо причин резко уменьшается количество эритроцитов и в связи с этим развивается кислородное голодание — гипоксия.
Законно предположить, что уменьшение снабжения организма кислородом автоматически приводит к увеличению продукции красных кровяных телец.
- Хорошо известно, что у жителей высокогорья, а так же у альпинистов, достигающих больших высот, число эритроцитов заметно повышается по сравнению с исходной нормой.
- И наоборот, если в барокамере создать повышенное давление кислорода, то через некоторое время можно отметить постепенное затухание, «вялость» красного кроветворения, вплоть до полного его прекращения.
Возникает вопрос о механизме «эритроцитостимулирующего» действия кислородного голодания. Большим количеством исследований установлено, что этот фактор убыстряет кроветворение через посредство особого вещества, стимулирующего эрицропоэз и получившего название «эритропоэтин».
В 1906 г. два французских исследователя — Карно и Дефляндер — обнаружили, что сыворотка крови, взятая у кроликов через 20 часов после массивной кровопотери и введенная другому здоровому кролику, способствовала у последнего приросту эритроцитов на 2—3 млн. в 1 мм3 крови, а также увеличению количества гемоглобина.
Последующие эксперименты показали, что кислородная недостаточность любого происхождения способна повышать эритростимулирующие свойства кровяной сыворотки.
Наиболее убедительные доказательства существования в организме стимулятора красного кроветворения были представлены в опытах на искусственно сращенных между собой (наподобие сиамских близнецов) крысах.
Этот интересный опыт выглядел так: одна из крыс дышала газовой смесью, содержащей пониженное количество кислорода, а ее партнер — воздухом с нормальным содержанием кислорода. И оказалось, что у обоих животных в костном мозге происходило одинаковое разрастание клеток «красного ряда», а в периферической крови — значительное увеличение эритроцитов.
Объяснить это можно следующим образом: у крысы под влиянием кислородного голодания образуется вещество эритростимулирующего действия, т. е. эритропоэтин, который переходит с кровью через сращенные кровеносные сосуды в организм партнера и вызывает у него активизацию кроветворения.
Особенности дифференцировки гемопоэтических клеток
Кроветворная ткань костного мозга объединяет в своем составе комбинацию морфологически нераспознаваемых гемопоэтических клеток-предшественниц и клеток специфических рядов дифференцировки. Все кроветворные клетки, нераспознаваемые с точки зрения морфологии – это гемопоэтические стволовые клетки, которые могут быть:
- мультипотентными (дифференцируются во всех направлениях);
- полипотентными (развиваются только по некоторым из них);
- унипотентными (следуют только по определенному пути развития).
Другая часть клеток, которые удается распознать морфологически, формируется путем дифференцировки из более молодых предшественников, стремительно развивающихся дальше.
Миелопоэз может протекать в нескольких направлениях:
- мегакариоцитарное;
- эритроцитарное;
- моноцитарное;
- гранулоцитарное.
Лимфопоэз включает в себя две основные линии дифференцировки – образование лимфоцитов Т- и В-клеточного ряда. Каждая из них проходит в два этапа. Первый из них является антиген-независимым и заканчивается продукцией структурно зрелых, но иммунологически неактивных лимфоцитов. Следующий этап начинается после контакта с потенциальным антигеном и завершается выработкой специализированных иммунных клеток (Т-киллеров, Т-хелперов, Т-супрессоров, плазматических клеток, клеток памяти).
Каждый ряд дифференцировки кроветворных клеток дебютирует со стадии так называемых «бластов» (например, миелобласты). Для обозначения клеток промежуточного этапа используют приставку «про» и суффикс «цит» (например, проэритрокариоцит). Зрелые клеточные элементы имеют только суффикс «цит» (например, тромбоцит).
Следует отметить, что процесс дифференцировки различных видов клеточных элементов имеет свои особенности. Так, в гранулоцитарном ряде выделяют не одну, а несколько промежуточных стадий. В этом случае вслед за миелобластом образуется промиелоцит, затем миелоцит, метамиелоцит, а только после этого – зрелые клетки – эозинофилы, базофилы, нейтрофилы.
Регуляция кроветворения
Адекватный и быстрый ответ системы кроветворения на вновь возникающие потребности организма в клетках крови обеспечивают цитокины.
В норме регуляция гемопоэза осуществляется непосредственным влиянием микроокружения и гуморальными факторами, обладающими активирующим или угнетающим действием. Эти факторы получили название цитокины. Они позволяют обеспечивать адекватный и быстрый ответ системы кроветворения на вновь возникающие потребности организма в клетках крови. К цитокинам активирующего типа относятся:
- факторы роста (колониестимулирующие);
- эритропоэтины;
- фактор стволовых клеток;
- интерлейкины и др.
Угнетают клеточную активность и кроветворение следующие субстанции:
- фактор некроза опухоли;
- интерферон-гамма;
- лейкоз-ингибирующий фактор и др.
При этом подавление роста одного вида клеток может приводить к усиленной дифференцировке другого.
Количество клеток в периферической крови регулируется по принципу обратной связи. Так, содержание эритроцитов в крови и насыщение их гемоглобином зависит от потребностей тканей в кислороде. Если она возрастает, то включаются не только компенсаторные механизмы (увеличение частоты дыхания и сердечных сокращений), но и стимулируется эритропоэз.
Что будет, если гемопоэз нарушится
К сожалению, встречаются заболевания, при которых нарушается одно или несколько звеньев производства крови. В зависимости от того, на каком уровне это произошло, тяжесть заболевания и его проявления будут варьировать.
Нарушение производства эритроцитов
Такое состояние возникает, если эритропоэз остановился до полного образования эритроцита. Основными проявлениями проблемы будут:
- снижение уровня гемоглобина в крови
- появление патологических форм гемоглобина
- повышенное разрушение недозрелых форм леток и, как
- следствие, появление желтухи
Нарушение производства лейкоцитов
Обычно такое нарушение связано с повышенной выработкой миелобластов или лимфоцитов, при этом развивается состояние знакомое всем как лейкоз. Клинически лейкоз появляется снижением общего иммунитета, присоединением множества инфекций и ненормальной реакцией организма на обычные процессы.
Нарушение производства тромбоцитов
Изменения в этом звене гемопоэза очень опасны, так как быстрее предыдущих ведут к гибели. Вся причина в том, что несовершенные тромбоциты не могут адекватно выполнить адгезивную функцию. Следовательно, даже малейшие повреждения будут сопровождаться массивными кровотечениями.
В заключении хочется сказать, что тонкие механизмы гемопоэза, практически не подвластны человеческому воздействию. Поэтому возникшие в них ошибки исправить бывает очень трудно.
Сен 29, 2016
Васкуляризация. Иннервация. Возрастные изменения. Регенерация.
Васкуляризация. Костный мозг снабжается кровью посредством сосудов, проникающих через надкостницу в специальные отверстия в компактном веществе кости. Войдя в костный мозг, артерии разветвляются на восходящую и нисходящую ветви, от которых радиально отходят артериолы. Сначала они переходят в узкие капилляры (2—4 мкм), а затем в области эндоста продолжаются в широкие тонкостенные с щелевидными порами синусы (диаметром 10—14 мкм). Из синусов кровь собирается в центральную венулу. Постоянное зияние синусов и наличие щелей в эндотелиальном пласте обусловливаются тем, что в синусах гидростатическое давление несколько повышено, так как диаметр выносящей вены меньше по сравнению с диаметром артерии. К базальной мембране с наружной стороны прилежат адвентициальные клетки, которые, однако, не образуют сплошного слоя, что создает благоприятные условия для миграции клеток костного мозга в кровь. Меньшая часть крови проходит со стороны периоста в каналы остеонов, а затем в эндост и синус. По мере контакта с костной тканью кровь обогащается минеральными солями и регуляторами кроветворения.
Кровеносные сосуды составляют половину (50%) массы костного мозга, из них 30% приходится на синусы. В костном мозге разных костей человека артерии имеют толстую среднюю и адвентициальную оболочки, многочисленные тонкостенные вены, причем артерии и вены редко идут вместе, чаще врозь.
Капилляры бывают двух типов: узкие 6—20 мкм и широкие синусоидные (или синусы) диаметром 200—500 мкм. Узкие капилляры выполняют трофическую функцию, широкие являются местом дозревания эритроцитов и выхода в кровоток разных клеток крови. Капилляры выстланы эндотелиоцитами, лежащими на прерывистой базальной мембране.
Иннервация. В иннервации участвуют нервы сосудистых сплетений, нервы мышц и специальные нервные проводники к костному мозгу. Нервы проникают в костный мозг вместе с кровеносными сосудами через костные каналы. Далее покидают их и продолжаются как самостоятельные веточки в паренхиме в пределах ячеек губчатого вещества кости. Они ветвятся на тонкие волоконца, которые либо вновь вступают в контакт с костномозговыми сосудами и оканчиваются на их стенках, либо заканчиваются свободно среди клеток костного мозга.
Возрастные изменения. Красный костный мозг в детском возрасте заполняет эпифизы и диафизы трубчатых костей и находится в губчатом веществе плоских костей. Примерно в 12—18 лет красный костный мозг в диафизах замещается желтым. В старческом возрасте костный мозг (желтый и красный) приобретает слизистую консистенцию и тогда называется желатинозным костным мозгом. Следует отметить, что этот вид костного мозга может встречаться и в более раннем возрасте, например при развитии костей черепа и лица.
Регенерация. Красный костный мозг обладает высокой физиологической и репаративной регенерационной способностью. Источником образования гемопоэтических клеток являются стволовые клетки, находящиеся в тесном взаимодействии с ретикулярной стромальной тканью. Скорость регенерации костного мозга в значительной мере связана с микроокружением и специальными ростстимулирующими факторами гемопоэза.
Некоторые термины из практической медицины:
- миелограмма (миело- + греч. gramma запись) — выраженный в форме таблицы или диаграммы результат микроскопии мазка пунктата костного мозга, отражающий качественный и количественный состав ядросодержащих клеток миелоидной ткани.;
- миелоидная реакция (миело- + греч. —eides подобный) — появление в периферической крови малодифференцированных клеток, относящихся к грануло- и эритропоэтическому ряду; наблюдается при метастазах злокачественной опухоли в костный мозг, а также при сепсисе, туберкулезе и некоторых других болезнях;
- остеомиелит (osteomyelitis; остео- + греч. myelos костный мозг + ит; син.: костоеда — устар., паностит) — воспаление костного мозга, обычно распространяющееся на компактное и губчатое вещество кости и надкостницу;
| Часть первая – Общая характеристика, классификация; красный костный мозг | immunesys1.mp37 122 кБ |
| Часть вторая – Вилочковая железа — тимус | immunesys2.mp35 310 кБ |
| Часть третья – Селезенка | immunesys3.mp36 073 кБ |
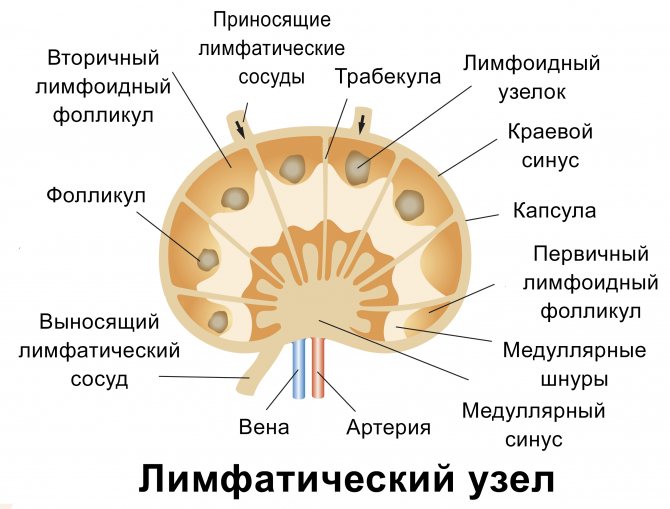
| Часть четвертая – Лимфатические узлы, лимфоидная ткань слизистых оболочек | immunesys4.mp37 152 кБ |
Что такое гемопоэз и последствия его нарушений
Кроветворение – это очень сложный процесс, он должен постоянно регулироваться и никак не изменяться. Любое изменение в ту или иную сторону приводит к нарушениям в организме и к возникновению различных заболеваний. Гемопоэз, что это такое и с чего он начинается, рассмотрим ниже.
В первые дни жизни эмбриона кроветворение происходит в стенках желчного мешка, в его утолщениях. Начало этого процесса приходится на 16-19 день развития, а после 60-го дня кроветворение начинает происходить в печени, селезенке и в тимусе. Затем, когда развился костный мозг (а он развивается самым последним из кроветворных органов), эти функции переходят к нему. Тогда в печени активное образование крови прекращается.
Как уже упоминалось выше, из стволовых клеток образуются миелоидные клетки (эритроциты, моноциты, тромбоциты, гранулоциты). Этот процесс получил название миелопоэз. Выработка предшественников лимфоидных клеток – лимфопоэз. Процесс миелопоэза осуществляется в миелоидной ткани, которая находится трубчатых, а также во многих губчатых костях. Во время миелопоэза происходит изменение типа клеток. Например, прежде чем стать тромбоцитами, меняется кариотип полиплоидных мегакариоцитов, а при образовании эритроцитов исчезает ядро у клеток эритробласт.
Селезенка, лимфатические узлы, тимус (вилочковая железа) и костный могз отвечают за протекание лимфопоэза. В лимфоидной ткани происходит образование лимфоцитов, плазмоцитов, а также удаляются клетки и остатки из распада.
При некоторых заболеваниях возникают нарушения в костном мозге, что приводит к нарушению кроветворения. Например, при увеличении количества тромбоцитов становится гуще кровь, что может привести к застою крови в различных органах, замедлению кровотока и образованию тромбов, что является большой опасностью для жизни человека.
Если же клеток крови вырабатывается недостаточно, то симптомы проявляются по мере того, как отмирают нормальные клетки. Самыми «маложивущими» являются гранулоциты, поэтому при их исчезновении организм становится более уязвимым для различных инфекций. Потом начинают убывать эритроциты, что проявляется в тромбоцитопении. Появляется кровоточивость. А при уменьшении количества эритроцитов характерными признаками являются бледность, общая слабость, одышка даже при, казалось бы, небольших нагрузках.
Познания в этой области улучшились только недавно, когда генная инженерия и культивирование клеток достигли нового уровня. Появилась возможность регулировать процесс кроветворения, подходя к этому индивидуально, в зависимости от того, сколько клеток недовырабатывается.
Следите за своим здоровьем! И будет не лишним узнать какие причины низкого гемоглобина в крови, и как бороться с проблемами такого характера.
Особенности процесса образования клеток крови: теории и факты
Процесс образования клеток крови идет непрерывно в течение всей человеческой жизни, интенсивность его строго соответствует потребностям организма.
По одной из современных теорий следует, что клетки крови человека — эритроциты, лейкоциты и тромбоциты происходят из единой родоначальной материнской клетки, так называемой «стволовой». Путем ее деления и развития появляются клепки, предопределяющие различные ветви кроветворения: образование эритроцитов, зернистых лейкоцитов (гранулоцитов), незернистых лейкоцитов (агранулоцитов), тромбоцитов.
Порожденная общей «стволовой» клеткой, каждая из этих ветвей имеет и свою собственную родоначальную клетку. В процессе деления и постепенного созревания и преобразования этих костномозговых элементов появляются зрелые клетки, поступающие в кровь.
К чести русской науки следует оказать, что мысль о происхождении всех клеток крови из единого источника принадлежит знаменитому русскому ученому-гистологу А. А. Максимову, создавшему еще в 1900—1914 гг. свою теорию кроветворения. Эти исследования нашли подтверждение и дальнейшее развитие в трудах советских исследователей.
Вместе с тем в некоторыми учеными высказывалась мысль о том, что еще до рождения человека в кроветворных органах предопределен вид каждой кроветворной линии — гранулоцитарной, эритроцитарной, лимфоцитарной. В пользу такой точки зрения приводятся данные биохимических исследований клеток крови и костного мозга.
Так, советские биохимики П. Ф. Сейц и П. С. Луганова обнаружили, что для определенных линий кроветворных элементов характерен определенный вид энергетического обмена. На основании этих данных они полагали, что и происхождение клеточных форм на каком-то этапе должно быть различным, поскольку характерный тип обмена (как группа крови, резус-фактор), возникший в клетке в начальном периоде ее развития, сохраняется во всех клеточных популяциях (производных данной линии).
Постэмбриональный гемопоэз
Постэмбриональный гемопоэз представляет собой процесс физиологической регенерации крови, который компенсирует физиологическое разрушение дифференцированных клеток. Он подразделяется на миелопоэз и лимфопоэз.
Миелопоэз происходит в миелоидной ткани, расположенной в эпифизах трубчатых и полостях многих губчатых костей. Здесь развиваются эритроциты, гранулоциты, моноциты, тромбоциты, а также предшественники лимфоцитов. В миелоидной ткани находятся стволовые клетки крови и соединительной ткани. Предшественники лимфоцитов постепенно мигрируют и заселяют тимус, селезенку, лимфоузлы и некоторые другие органы.
Лимфопоэз происходит в лимфоидной ткани, которая имеет несколько разновидностей, представленных в тимусе, селезенке, лимфоузлах. Она выполняет функции образования T- и B-лимфоцитов и иммуноцитов (например, плазмоцитов).
Миелоидная и лимфоидная ткани являются разновидностями соединительной ткани, т.е. относятся к тканям внутренней среды. В них представлены две основные клеточные линии — клетки ретикулярной ткани и гемопоэтические клетки.
Ретикулярные, а также жировые, тучные и остеогенные клетки вместе с межклеточным веществом формируют микроокружение для гемопоэтических элементов. Структуры микроокружения и гемопоэтические клетки функционируют в неразрывной связи друг с другом. Микроокружение оказывает воздействие на дифференцировку клеток крови (при контакте с их рецепторами или путем выделения специфических факторов).
Таким образом, для миелоидной и всех разновидностей лимфоидной ткани характерно наличие стромальных и гемопоэтических элементов, образующих единое функциональное целое.
СКК относятся к самоподдерживающейся популяции клеток. Они редко делятся. Выявление СКК стало возможным при применении метода образования клеточных колоний – потомков одной стволовой клетки.
Пролиферативную активность СКК регулируют колониестимулирующие факторы (КСФ), различные виды интерлейкинов (ИЛ-3 и др.).
Каждая СКК в эксперименте или лабораторном исследовании образует одну колонию и называется колониеобразующей единицей (сокращенно КОЕ, CFU).
Исследование клеточного состава колоний позволило выявить две линии их дифференцировки.
Одна линия дает начало мультипотентной клетке — родоначальнице гранулоцитарного, эритроцитарного, моноцитарного и мегакариоцитарного рядов гемопоэза (сокращенно КОЕ-ГЭММ).
Вторая линия дает начало мультипотентной клетке — родоначальнице лимфопоэза (КОЕ-Л).
Из мультипотентных клеток дифференцируются олигопотентные (КОЕ-ГМ) и унипотентные родоначальные клетки.
Методом колониеобразования определены родоначальные унипотентные клетки для моноцитов (КОЕ-М), нейтрофильных гранулоцитов (КОЕ-Гн), эозинофилов (КОЕ-Эо), базофилов (КОЕ-Б), эритроцитов (БОЕ-Э и КОЕ-Э), мегакариоцитов (КОЕ-МГЦ), из которых образуются клетки-предшественники. В лимфопоэтическом ряду выделяют унипотентные клетки — предшественницы для B-лимфоцитов и для T-лимфоцитов. Полипотентные (плюрипотентные и мультипотентные), олигопотентные и унипотентные клетки морфологически не различаются.
Все приведенные выше стадии развития клеток составляют четыре основных класса, или компартмента, гемопоэза:
- I класс — СКК — стволовые клетки крови (плюрипотентные, полипотентные);
- II класс — КОЕ-ГЭММ и КОЕ-Л — коммитированные мультипотентные клетки (миелопоэза или лимфопоэза);
- III класс — КОЕ-М, КОЕ-Б и т.д. — коммитированные олигопотентные и унипотентные клетки;
- IV класс — клетки-предшественники (бласты, напр.: эритробласт, мегакариобласт и т.д.).
Сразу отметим, что оставшиеся два класса гемопоэза составляют созревающие клетки (V класс) и зрелые клетки крови (VI класс).
Эритропоэз у млекопитающих и человека протекает в костном мозге в особых морфофункциональных ассоциациях, получивших название эритробластических островков.
Эритробластический островок состоит из макрофага, окруженного одним или несколькими кольцами эритроидных клеток, развивающихся из унипотентной КОЕ-Э, вступившей в контакт с макрофагом. КОЕ-Э и образующиеся из нее клетки (от проэритробласта до ретикулоцита) удерживаются в контакте с макрофагом его рецепторами.
У взрослого организма потребность в эритроцитах обычно обеспечивается за счет усиленного размножения эритробластов. Но всякий раз, когда потребность организма в эритроцитах возрастает (например, при потере крови), эритробласты начинают развиваться из предшественников, а последние — из стволовых клеток.
В норме из костного мозга в кровь поступают только эритроциты и ретикулоциты.
Назначение схемы гемопоэза
Схема гемопоэза
Все выше сказанное можно объединить в единую схему.
Назначение такой схемы трудно переоценить. Она имеет огромное количество плюсов и несомненную значимость.
- При помощи такой схемы можно отчетливо отследить все этапы образования интересующей клетки.
- Если нужная клетка не образовалась, можно отследить на каком этапе произошла ошибка и цепочка действий прервалась.
- Найдя ошибку в системе, врач может воздействовать на интересующее звено кроветворения, чтобы его простимулировать.
Таким образом, схема гемопоэза ясно представляет структуру периферической крови по компонентам, что также немаловажно в диагностике патологических процессов
Роль витамина В12 в кроветворении
В кроветворении принимают участие различные витамины, среди которых особая роль принадлежит витамину В12, содержащему кобальт.
Источником витамина В12 служат продукты животного происхождения; в растительных продуктах он отсутствует. Благодаря этому витамину поддерживается нормальный процесс созревания эритроцитов у здорового человека.
В сутки взрослому человеку необходимо 3—5 мг витамина В12. Как показали современные исследования, витамин В12, попавший в организм с пищей, всасывается в кишечнике лишь при соединении его с особым белком — гастромукопротеином (который иначе называется «внутренний фактор»).
Гастромукопротеин вырабатывается у человека железами желудка и обладает способностью образовывать с витамином В12 комплексное соединение. Оказалось, что этот белок предохраняет витамин от пожирания микроорганизмами, заселяющими кишечник. Таким образом, он выступает в роли «проводника» витамина В12 и спасает его от разрушающего действия микробов.
Всосавшийся витамин накапливается в печени и затем используется для целей кроветворения по мере необходимости.
Установлено, что витамин B12 принимает активное участие в образовании соединений, являющихся составными частями нуклеиновых кислот, — тех самых кислот, коими так богаты ядра клеток и которые определяют основные наследственные признаки организма.
В случае нехватки витамина B12 задерживается синтез нуклеиновых кислот, в результате чего неизбежно нарушается деление постоянно размножающихся кроветворных клеток. Тогда в костном мозге вместо нормальных эритробластов появляются огромные, медленно созревающие клетки, получившие название мегалобластов (от греческого слова «мегалос» — огромный).
Гемопоэтическая стволовая клетка
Стволовые клетки обладают замечательным потенциалом дифференцироваться во многие различные типы клеток в организме. Кроме того, во многих тканях они служат своеобразной ремонтной средой. Стволовые клетки отличаются от других двумя важными характеристиками. Во-первых, они являются неспециализированными клетками и способны к регенерации путем деления клеток даже после длительных периодов бездействия. Во-вторых, при определенных условиях они могут быть вызваны определенными факторами, чтобы дифференцироваться в специфичные для органа клетки со специальными функциями.
Клетки крови образуются гемопоэтическими стволовыми клетками в результате процессов пролиферации и дифференцировки. Дифференциация регулируется факторами роста и цитокинами, которые выделяются клетками в микроокружении. После начала процессов дифференцировки гемопоэтические стволовые клетки теряют способность к самообновлению. Они могут дифференцироваться в клетки-предшественники, которые могут стать клетками крови в двух основных категориях: миелоидная линия или лимфоидная линия. После нескольких делений получают унипотентные клетки-предшественники, которые способны дифференцироваться только в одну клеточную линию – гранулоцит-моноцит, эритроид, мегакариоцит, B- или T-лимфоцит.
Контроль гемоцитопоэза
Гемоцитопоэз объединяет процессы, связанные с преобразованием различных клеток в зрелые элементы крови. Так обеспечивается естественное сокращение лишнего количества форменных элементов. Полипотентные стволовые клетки самостоятельно проходят регенерацию. Они могут образовываться вне органов кроветворения. При стандартной дифференциации полипотентные клетки, сосредоточенные в костном мозге, способствуют зарождению зрелых элементов крови. Это:
- базофилы;
- эритроциты;
- различные типы лимфоцитов;
- эозинофилы;
- нейтрофилы.
К ним относят:
- попадание инфекции в организм;
- механические повреждения и другие факторы, способствующие потере определенного количества крови;
- адаптация к условиям высокогорья.
Что представляет собой процесс кроветворения и где он происходит
Сам по себе гемопоэз — это многоэтапная последовательность получения взрослых кровяных клеток из клеток, которые являются их предшественниками и в норме не встречаются в циркулирующей по сосудам крови. Зрелыми называются клетки, которые обычно обнаруживаются в нормальном анализе крови человека.
Человеческие клетки
Где же происходят все эти сложные процессы? Клетки предшественницы образуются в ряде органных структур человеческого тела.
- Основным коллектором кроветворных процессов является костный мозг. Все действо идет в полостях костей, где находится стромальное микроокружение. К частичкам такого окружения относятся клетки, выстилающие сосуды, фибробласты, костные клетки, жировые и многие другие. Все, что их окружает, состоит из белков, различных волокон, между которыми находится основное костное вещество. В строме есть адгезивная составляющая, которая как бы притягивает основные кроветворящие клетки. Самые «первые» структуры схемы гемопоэза находятся в костном мозге. Родоначальники лимфоцитов образуются здесь же, а дозревают потом в вилочковой железе и селезенке, а также в лимфоузлах.
- Селезенка – еще один немаловажный орган. Она состоит из красной и белой зон. В красной зоне складируются и разрушаются эритроциты, в белой зоне обитают т-лимфоциты. Склады в-лимфоцитов находятся по окружности от красной зоны.
- Вилочковая железа – основной «завод» по производству лимфоцитов. Туда попадают из костного мозга недозрелые клетки. В тимусе они очень быстро преобразуются, большая часть из них гибнет, а выжившие превращаются в хелперов и супрессоров и направляются к селезенке и лимфоузлам. Чем старше человек, тем меньше его вилочковая железа. Со временем она полностью редуцируется, становясь комком жира.
- Лимфоузлы – это так называемые иммунные ответчики, которые за счет предоставления антигена первые реагируют на изменения в иммунитете. По периферии узла находятся Т-лимфоциты, а в сердцевине – зрелые клетки.
- Пейеровы бляшки – аналог узлов, только расположены они по ходу кишечника.
Таким образом, практически все органы напрямую или косвенно связаны с кроветворением.
Регуляция гемопоэза
Кроветворение регулируется:
- факторами роста, обеспечивающими пролиферацию и дифференцировку СКК и последующих стадий их развития,
- факторами транскрипции, влияющими на экспрессию генов, определяющих направление дифференцировки гемопоэтических клеток,
- витаминами, гормонами.
Факторы роста включают колониестимулирующие факторы (КСФ), интерлейкины и ингибирующие факторы. Они являются гликопротеинами, действующими и как циркулирующие гормоны, и как местные медиаторы, регулирующие гемопоэз и дифференцировку специфических типов клеток. Почти все факторы роста действуют на СКК, КОЕ, коммитированные и зрелые клетки. Однако отмечаются индивидуальные особенности действия этих факторов на клетки-мишени.
КСФ действуют на специфические клетки или группы клеток на различных стадиях дифференцировки. Например, фактор роста стволовых клеток влияет на пролиферацию и миграцию СКК в эмбриогенезе. В постнатальном периоде на гемопоэз оказывают влияние несколько КСФ, среди которых наиболее изучены факторы, стимулирующие развитие гранулоцитов и макрофагов (ГМ-КСФ, Г-КСФ, М-КСФ), а также интерлейкины.
Большинство указанных факторов выделено и применяется для лечения различных болезней. Для получения их используются биотехнологические методы.
Дифференцировка полипотентных клеток в унипотентные определяется действием ряда специфических факторов, поэтинов — эритропоэтинов (для эритробластов), гранулопоэтинов (для миелобластов), лимфопоэтинов (для лимфобластов), тромбопоэтинов (для мегакариобластов).
Большая часть эритропоэтина образуется в почках. Его образование регулируется содержанием в крови кислорода, которое зависит от количества циркулирующих в крови эритроцитов. Снижение числа эритроцитов и соответственно парциального давления кислорода, является сигналом для увеличения продукции эритропоэтина. Эритропоэтин действует на чувствительные к нему КОЕ-Э, стимулируя их пролиферацию и дифференцировку, что в конечном итоге приводит к повышению содержания в крови эритроцитов.
Тромбопоэтин синтезируется в печени, стимулирует пролиферацию КОЕ-МГЦ, их дифференцировку и образование тромбоцитов.
Ингибирующие факторы дают противоположный эффект, т.е. тормозят гемопоэз; их недостаток может быть одной из причин лейкемии, характеризующейся значительным увеличением числа лейкоцитов в крови. Выделен ингибирующий лейкемию фактор (ЛИФ), который тормозит пролиферацию и дифференцировку моноцитов-макрофагов.
Витамины необходимы для стимуляции пролиферации и дифференцировки гемопоэтических клеток. Витамин В12 поступает с пищей и соединяется с внутренним фактором (Касла), который синтезируется париетальными клетками желудка. Образуемый при этом комплекс, в присутствии ионов Са2+, соединяется с рецепторами эпителиоцитов подвздошной кишки и всасывается. При всасывании в эпителиоциты поступает лишь витамин В12, а внутренний фактор освобождается. Витамин В12 поступает с кровью в костный мозг, где влияет на гемопоэз, и в печень, где может депонироваться. Нарушение процесса всасывания при различных заболеваниях желудочно-кишечного тракта может служить причиной дефицита витамина В12 и нарушений в гемопоэзе.
Некоторые термины из практической медицины:
- анемия (син. малокровие) — состояние, характеризующееся снижением содержания гемоглобина в единице объема крови, чаще при одновременном уменьшении количества эритроцитов;
- анемия ахрестическая — общее название анемий, развивающихся вследствие неспособности эритробластов костного мозга использовать какие-либо антианемические факторы (цианокобаламин, фолиевую кислоту, железо и др.) при их нормальном поступлении в организм;
- хлороз ранний (син.: бледная немочь, хлороз ювенильный) — железодефицитная анемия у девушек в период полового созревания, проявляющаяся алебастровой бледностью кожи с зеленоватым оттенком, извращением вкуса, олигоменореей;
- хлороз поздний (син. анемия железодефицитная эссенциальная) — железодефицитная анемия у женщин в возрасте старше 30 лет, обычно связанная с маточными или другими кровотечениями, проявляющаяся извращением вкуса и обоняния, признаками атрофии слизистой оболочки полости рта и пищевода, выпадением волос, искривлением ногтей, позже — выраженными признаками анемии;